
【题目】苹果酸广泛存在于苹果等水果的果肉中是一种常用的食品添加剂。经测定,草果酸的相对分子质量为134,所含各元素的质量分数为w(C)=35.82%,w(H)=4.48%、w(O)=59.70%。其中存在5种不同化学环境的H原子。以乙烯为原料人工合成草果酸的线路如图所示:
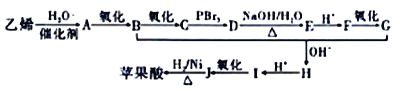
已知:①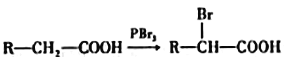
②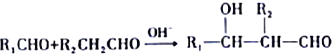
请回答下列问题:
(1)苹果酸的分子式为_______,B物质的名称为_______。F中含有的官能团名称是_______。
(2)G+B→H的反应类型是____________。I 的结构简式为___________________。
(3)D→E反应的化学方程式为________________________________。
(4)1mol苹果酸能与________molNaHCO3完全反应,能与足量的Na反应生成_______LH2(标况下)。
(5)与苹果酸含有相同种类和数量的官能团的同分异构体的结构简式为_________;其所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是__________(填序号)。
a. 元素分析仪 b.红外光谱仪 c. 质谱仪 d.核磁共振仪
【答案】 C4H6O5 乙醛 羟基、羧基 加成反应 HOOC-CH(OH)-CH2CHO BrCH2COOH+2NaOH![]() HOCH2COONa+NaBr+H2O 2 33.6
HOCH2COONa+NaBr+H2O 2 33.6 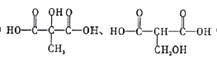 ac
ac
【解析】本题主要考查有机物的结构与性质。
(1)草果酸分子中含有的碳原子数、氢原子数、氧原子数分别为:134×35.82%/12=4、134×4.48%=6、134×59.70%/16=5。苹果酸的分子式为C4H6O5,B是乙醇的氧化产物,B物质的名称为乙醛。F中含有的官能团名称是羟基、羧基。
(2)G+B→H的反应类型是加成反应。I 的结构简式为HOOC-CH(OH)-CH2CHO。
(3)D→E反应的化学方程式为BrCH2COOH+2NaOH![]() HOCH2COONa+NaBr+H2O。
HOCH2COONa+NaBr+H2O。
(4)苹果酸分子含有两个羧基和一个羟基,羧基可NaHCO3与反应,羟基(包括羧基中羟基)可与Na反应,所以1mol苹果酸能与2molNaHCO3完全反应,能与足量的Na反应生成1.5mol即33.6LH2(标况下)。
(5)与苹果酸含有相同种类和数量的官能团的同分异构体的结构简式为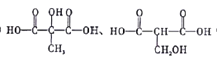 ;其所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是ac。a. 用来分析有机物的元素含量;b.用来测定有机物的结构;c.用来测定有机物的相对分子质量; d.用来测定有机物的氢原子的种类。故选ac.
;其所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是ac。a. 用来分析有机物的元素含量;b.用来测定有机物的结构;c.用来测定有机物的相对分子质量; d.用来测定有机物的氢原子的种类。故选ac.


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】现有以下几种有机物:
![]()

![]() 癸烷
癸烷 ![]()
![]()
![]()
![]()
![]()
![]()

![]() 丙烷
丙烷
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃的结构简式为__________________;
(2)与③互为同分异构体的是_________(填序号),③在光照的条件下与氯气发生反应生成的一氯代物结构有__________种;
(3)有机物②在加热条件下和CuO反应的化学方程式__________________________;
(4)用“![]() ”表示
”表示![]() 熔沸点高低顺序:____________(填序号);
熔沸点高低顺序:____________(填序号);
(5)有机物②和与它相对分子质量相同的饱和一元羧酸发生酯化反应的化学方程式___________________________________________________;
(6)在![]() ,
,![]() 条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是___________(填序号);它与
条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是___________(填序号);它与![]() 互为___________关系。
互为___________关系。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列有关说法不正确的是
A. 由1mol CH3OCOONa和少量CH3COOH形成的中性溶液中,CH3COO-数目是NA
B. 1.68gFe与足量高温水蒸气反应,转移电子的数目为0.09NA
C. 氢原子数为0.4NA的CH3OH 分子中含有的电子数为1.8NA
D. 常温下,2L 0.1molL-1FeCl3溶液与1L0.2molL-1FeCl3溶液所含Fe3+数目不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是
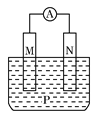
M | N | P | |
A | Zn | Cu | 稀H2SO4溶液 |
B | Cu | Fe | 稀HCl溶液 |
C | Ag | Zn | AgNO3溶液 |
D | Zn | Fe | Fe(NO3)3溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在容积恒定的密闭容器中,进行可逆反应:A(s)+2B(g) ![]() C(g)+D(g),当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
C(g)+D(g),当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
A.容器内气体的压强
B.混合气体的总物质的量
C.A的物质的量浓度
D.混合气体的平均相对分子质量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池叙述正确的是( )
A.水果电池是高效环保的家用电池
B.锌锰干电池是一种常用的二次电池
C.锌锰干电池碳棒是负极,锌片是正极
D.锌锰干电池工作一段时间后锌外壳逐渐变薄
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铝分别和O2、O3发生反应生成Al2O3 , 反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。下列有关说法中不正确的是( )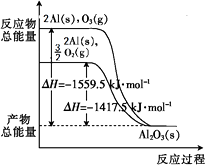
A.Al(s)与O3(g)反应的热化学方程式为2Al(s)+O3(g)=Al2O3(s) ΔH =-1559.5 kJ·mol-1
B.等质量的O2比O3的能量低
C.1 mol O2完全转化为O3 , 需吸收142 kJ的热量
D.给3O2(g) ![]() 2O3(g)的平衡体系加热,有利于O3的生成
2O3(g)的平衡体系加热,有利于O3的生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一固定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2 ![]() 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2 , 气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2 , 气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
(1)判断该反应达到平衡状态的标志是。(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.向装置中再充入SO3
(3)求该反应达到平衡时SO2的转化率为(用百分数表示)。
(4)若将平衡混合气体的5%通入过量的Ba(OH)2溶液,生成沉淀。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com