
����Ŀ���л���A����ͼ��ʾ��ת����ϵ��

��֪�����л���B�Ƿ������ĺ������������Է�������Ϊ108��B��������������Ϊ14.8%��
��![]() ��
��
��G����ʽ��C18H16O4 ���ṹ�к���3����Ԫ����
����������Ϣ���ش��������⣺
��1�����E���������������_____________��
��2��A�Ľṹ��ʽΪ_____________��
��3��������Ϊ_____________��E��H��D��F�ķ�Ӧ���ͷֱ�Ϊ_____________��_____________��
��4��Q��N��ͬϵ���Է���������N��14��Q�ж���ͬ���칹�壬��ͬʱ��������������ͬ���칹����_____________�֣����к˴Ź�������Ϊ4��壬�ҷ����֮��Ϊ3:2:2:1���л���ṹ��ʽΪ_____________��
a�����б��� b���ܷ���������Ӧ c����FeCl3��Һ������ɫ d���������Ѽ�
��5��д������ת���Ļ�ѧ����ʽ��
B��M__________________________
F��G__________________________
���𰸡� �Ȼ� ![]() Ũ���ᡢ���� �Ӿ۷�Ӧ ȡ����Ӧ��ˮ�ⷴӦ�� 8
Ũ���ᡢ���� �Ӿ۷�Ӧ ȡ����Ӧ��ˮ�ⷴӦ�� 8 ![]() 2
2 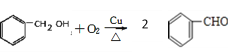 + 2 H2O
+ 2 H2O 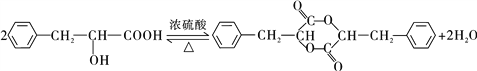
���������л���B�Ƿ������ĺ������������Է�������Ϊ108��B��������������Ϊ14.8%��B��Oԭ�Ӹ���=108��14.8%/16=1��̼ԭ�Ӹ���=(10816)/12=7��8������B����ʽΪC7H8O��B�к��б���������������������BΪ![]() ��B������������M��MΪ
��B������������M��MΪ![]() ��NΪ�����ᣬ�ṹ��ʽΪ
��NΪ�����ᣬ�ṹ��ʽΪ![]() ��A����ˮ�ⷴӦ���ɴ������ᣬCΪ���ᣬ���������Ϣ֪��C����ȡ����Ӧ����D��D������ӦȻ���ữ�õ�E��E������H��D�Ǻ�����ԭ�ӵ����ᣬ��D���������ƵĴ���Һ�м�������E��E�����Ӿ۷�Ӧ����H������DΪ
��A����ˮ�ⷴӦ���ɴ������ᣬCΪ���ᣬ���������Ϣ֪��C����ȡ����Ӧ����D��D������ӦȻ���ữ�õ�E��E������H��D�Ǻ�����ԭ�ӵ����ᣬ��D���������ƵĴ���Һ�м�������E��E�����Ӿ۷�Ӧ����H������DΪ ��EΪ
��EΪ![]() ��CΪ
��CΪ![]() ��D��Ӧ����F��F�ܷ�Ӧ����E����D����ˮ�ⷴӦ����F��FΪ
��D��Ӧ����F��F�ܷ�Ӧ����E����D����ˮ�ⷴӦ����F��FΪ ��F����������Ӧ����G������G����ʽ֪��GΪ
��F����������Ӧ����G������G����ʽ֪��GΪ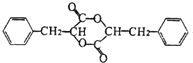 ������B��C�ṹ��ʽ֪��AΪ
������B��C�ṹ��ʽ֪��AΪ![]() ����
����
��1��EΪ![]() ��E�к����������������Ȼ�����2��A�Ľṹ��ʽΪ
��E�к����������������Ȼ�����2��A�Ľṹ��ʽΪ![]() ����3��ͨ�����Ϸ���֪��������ΪŨ���ᡢ���ȣ�E��H�ķ�Ӧ����Ϊ�Ӿ۷�Ӧ��D��F�ķ�Ӧ����Ϊȡ����Ӧ��ˮ�ⷴӦ������4��NΪ
����3��ͨ�����Ϸ���֪��������ΪŨ���ᡢ���ȣ�E��H�ķ�Ӧ����Ϊ�Ӿ۷�Ӧ��D��F�ķ�Ӧ����Ϊȡ����Ӧ��ˮ�ⷴӦ������4��NΪ![]() ��Q��N��ͬϵ���Է���������N��14����Q�к����Ȼ����ҷ�����̼ԭ������N��һ��������������a�����б�����b���ܷ���������Ӧ��˵����ȩ��c����FeCl3��Һ������ɫ��˵�������з��ǻ���d.�������Ѽ��������������Q�ĽṹΪ����������HCOO-��-CH3��������-CHO��-CH2OH��ÿ�ֶ����ڼ�����֣��������1��ȡ��������������CH2OOCH����CHOHCHO�����Թ���8�֣����к˴Ź�������Ϊ4��壬�ҷ����֮��Ϊ3��2��2��1���л���ṹ��ʽΪ
��Q��N��ͬϵ���Է���������N��14����Q�к����Ȼ����ҷ�����̼ԭ������N��һ��������������a�����б�����b���ܷ���������Ӧ��˵����ȩ��c����FeCl3��Һ������ɫ��˵�������з��ǻ���d.�������Ѽ��������������Q�ĽṹΪ����������HCOO-��-CH3��������-CHO��-CH2OH��ÿ�ֶ����ڼ�����֣��������1��ȡ��������������CH2OOCH����CHOHCHO�����Թ���8�֣����к˴Ź�������Ϊ4��壬�ҷ����֮��Ϊ3��2��2��1���л���ṹ��ʽΪ![]() ����5��B��M�������Ĵ���������Ӧ����ʽΪ
����5��B��M�������Ĵ���������Ӧ����ʽΪ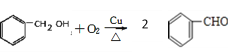 + 2 H2O ��F����������Ӧ����G����Ӧ����ʽΪ
+ 2 H2O ��F����������Ӧ����G����Ӧ����ʽΪ ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������м��ַ�Ӧ���ͣ� ����ȥ ��ȡ�� �������ܼӳ� �ݻ�ԭ ��ˮ�⣬�ñ�ȩ��ȡ 1��2�������� ��![]() ��������ȷ�ĺϳ�·�����η����ķ�Ӧ�������Ͳ������ǣ� ��
��������ȷ�ĺϳ�·�����η����ķ�Ӧ�������Ͳ������ǣ� ��
A. �ݢ٢ܢ� B. �ܢ٢ܢ� C. �ݢ٢ܢ� D. �ݢۢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��к͵ζ��IJ��������²�����ȷ��˳����___��
���ñ�Һ��ϴ�ζ��ܣ������ζ�����ע�����Һ���ۼ��ζ����Ƿ�©ˮ���ܵζ����ݵμ�ָʾ���ڴ���Һ����ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϡ���������ҹ�ս������Դ����̼�����Ҫ��ѧ�ɷ�ΪCeFCO3��������ȡ����ϡ��Ԫ�ص���Ҫ����ԭ�ϡ�����һ����ȡ��Ĺ����������£�

��֪�����պ������к���4�۵��漰+3�۵�����ϡ���������+ 4�۵�����������к�ǿ�������ԣ�ͨ���������������ױ���ԭ����ԭ�ɣ�3�۶�����ˮ����ش���������
��1�����l�����õ���AΪ������ĸ��ʾ��________��a������ b��ϡ���ᣩ��ԭ����_______��
��2���������Ϊ�������������ķ���������ʽ��ʧ�����ÿ����Լ��ν��ķ���������ӳ�����ȥ���÷�Ӧ�����ӷ���ʽΪ___________��
��3��ʵ�����н�����ȡ�������õ�����Ҫ��������������________���ڲ���I�����Һ�м���NaOH��Һ��Ϊ�˵�����ҺpH ���Ce(OH)3��_______���ⶨ����ҺpH�IJ�����_______��
��4��д����������Ļ�ѧ����ʽ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
�������漰�л��������˵������ȷ���� ______________________
A����ȥ��������������ϩ��ͨ������KMnO4��Һ���з���
B���ױ������ƶ������ױ��뱽������Ҵ���Ӧ�Ʊ����������ķ�Ӧ���Ͳ�ͬ
C��������������Һ�������ͺ�����
D����ȥ�Ҵ��������������������ʯ�ң�����
E����ȥ��������������������ñ�������������Һϴ�ӡ���Һ���������
������ȩ��������õ�����������ȩ��1-������Ʒ��Ϊ����1-��������С���������֪����R-CHO+NaHSO3�����ͣ���RCH��OH��SO3Na����
�ڷе㣺����34�棬1-����118�棬����Ƴ������ᴿ·�ߣ�
![]()
��1���Լ�1Ϊ__________������2Ϊ__________������3Ϊ__________��
��2��д������ȩ������Ӧ����ʽ___________________________________
����֪��1,2-��������������Ϳ����������Ӽ�,������������ɫҺ��,�ܶ���2.18��/����3,�е�131.4��,�۵�9.79��,������ˮ,�����ڴ����ѡ���ͪ���л��ܼ�����ʵ���п�������ͼ��ʾװ���Ʊ�1,2-�������顣���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ,�Թ�d��װ��Һ��(���渲������ˮ���������ж�)������д���пհף�
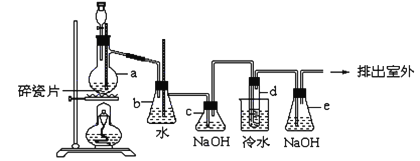
��1��д���Ʊ�1,2-��������Ļ�ѧ����ʽ����________________________________��
��2����ȫƿb���Է�ֹ����,�����Լ��ʵ�����ʱ�Թ�d�Ƿ�����������д����������ʱƿb�е�����_______________________________________��
��3��cװ����NaOH��Һ��������______________________________��
��4��eװ����NaOH��Һ��������_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A�Ǻ�4̼�Ķ�����ŵ����������1molA����2molH2���мӳɣ�A��̼��û��֧����F�ķ���ʽΪC4H6O2������ͼʾ���

��1��������A���еĹ����ţ����ƣ���____________________________________��
��2����A������ͬ�����ŵ�A��ͬ���칹��Ľṹ��ʽ��________________��
��3��B���ữ����Br2��Ӧ�õ�D��д������D�ķ�Ӧ��ѧ����ʽ__________________��
��4��F�Ľṹ�ü���ʽ��ʾ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���A��B��C��D��E��F��ת����ϵ��

��֪��Ϣ��
��23 g A��ȫȼ�����ɵ���������ͨ��Ũ����������ij���ʯ��ˮ�����Ũ��������
27 g������ʯ��ˮ����100 g�������ɡ�
��A������ƿ���������Ӧ����������
��B��һ��ֲ���������ڼ�������ˮ���������������ƽ��ṹ��
��F��һ����ɫ��״����ζ��Һ�塣
��ش��������⣺
(1)A�Ľṹ��ʽΪ________________��
(2)A��E��F�Ļ�ѧ����ʽΪ________________________________________���÷�Ӧ������________________��Ӧ��
(3)B��A�Ļ�ѧ����ʽΪ__________________________________________��
(4)E�к���ԭ���ŵ�����Ϊ________��д��E�������������е�һ��Ӧ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӫ���ḻ�����С��߲�֮���������ơ�������������˶���ͬʳ���ý�ʯ��ij��ѧ��ȤС��ԡ����˶����Ƿ���ͬʳ�������������̽����
���������ϡ��ٲ��˺��зḻ�����������Ρ�̼���εȣ������к��зḻ�ĵ����ʼ����Ρ�
�������ʯ����Ҫ�ɷ֣�����ƣ�CaC2O4��
�۴�������Ʒ�Ӧ��������̼��Ʒ�Ӧ���ɿ������εȡ�
��������롿�����˶�������ͬʳ����ԭ�������____________��
��̽��һ�������в��ֳɷַ���

��1����������жϼ����CaCl2��Һ�������ķ�����___________��
��2����֪����C��ʹ����ʯ��ˮ����ǣ�����Ļ�ѧʽ��HAc��ʾ��д������ܵĻ�ѧ��Ӧ����ʽ________________������A��B��������ϵΪ��m��A��_________m��B�������������������������
��3����ɫ����B�Ļ�ѧʽΪ_________���ɴ˿ɼ����˶�������ͬʳ��������ʳ�۵���ȷ����__________������ĸ��
A�����Բ��� B���߸�ţ�̿��벤��ͬʳ
C���������ʱ���ÿ�ˮ�̣��ɽ��Ͳ����κ���
��̽������ij����ƾ��壨CaC2O4��xH2O���ȷֽ��о�
(��ʾ��CaC2O4��xH2O���Ȼ�ʧȥ�ᾧˮ��ΪCaC2O4 ����ɫ����ͭ��ĩ��ˮ���������
����ͼװ�ý�����ƾ�����Ʒ���¼��ȣ�ʹ����ȫ�ֽ⣬����������������̽��������װ���и��Լ���������

��4���ٷ�Ӧ��ʼǰͨ�뵪����Ŀ����___________��װ��C��������_______________��
��װ��B������ͭ��ĩ������C��F�г���ʯ��ˮ������ǣ�E��CuO��죬˵��������__________________��������A�в�������Ϊ�����
�۶�����װ�ôӻ����Ƕ���һ���Ľ�����_____________��
��5��ij�о�������SDT Q600�ȷ����ǶԲ���ƾ��壨CaC2O4��xH2O�������ȷֽ⣬
���������ݣ����Ƴɹ����������ֽ��¶ȵĹ�ϵ��ͼ��

��800������ʱ������ɷֵĻ�ѧʽΪ_______��
�ڲ�������ΪCaC2O4ʱ���¶ȷ�Χ__________��
��д������������12.8g��Ϊ10.0gʱ�Ļ�ѧ����ʽ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͼ�����������ȷ����
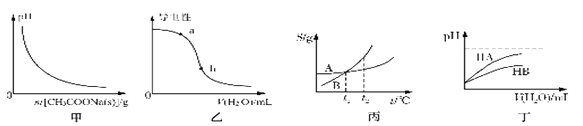
A. ͼ�ױ�ʾ��CH3COOH��Һ������CH3COONa�������ҺpH �ı仯
B. ͼ�ұ�ʾ�������Һ�м�ˮʱ�䵼���Ա仯����CH3COOH��Һ��pH: a>b
C. ͼ����ʾA��B�����ʵ��ܽ�����¶ȱ仯�������A��B ������Һ�ֱ���t1��������t2�� ʱ�����ʵ���������A=B
D. ͼ����ʾ�����£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯����ͬŨ�ȵ�NaA��Һ��pH����NaB��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com