
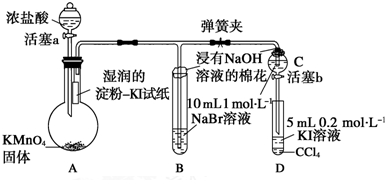
分析 装置A中是高锰酸钾固体和滴入的盐酸反应生成氯气,氯气和KI反应生成I2,I2单质遇到淀粉变蓝色,生成的氯气通入装置B中和NaBr反应生成溴单质,证明氯气氧化性大于溴,通过装置C排除Cl2对溴置换碘实验的干扰,溴单质和碘化钾反应生成碘单质,在四氯化碳中呈紫红色,证明溴单质氧化碘单质,
(1)根据氧化剂的氧化性大于氧化产物的氧化性,并检验产物碘;
(2)B中氯气与溴离子发生氧化还原反应生成溴单质和氯离子;
(3)根据氧化剂的氧化性大于氧化产物的氧化性,并检验产物碘的存在;
(4)为验证溴的氧化性强于碘,实验时应避免氯气的干扰;
(5)从原子结构(电子层数、原子半径)的角度分析.
解答 解:(1)因Cl2的氧化性大于I2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,可发生:Cl2+2I-=I2+2Cl-,I2能使淀粉变蓝,
故答案为:淀粉KI试纸变蓝;
(2)因Cl2的氧化性大于Br2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,可发生:Cl2+2Br-=Br2+2Cl-,
故答案为:Cl2+2Br-=Br2+2Cl-;
(3)因Cl2的氧化性大于I2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,会发生反应:Br2+2I-=I2+2Br-,同时检验产物碘的存在,所以为验证溴的氧化性强于碘,过程Ⅳ的操作和现象为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡.静置后CCl4层溶液变为紫红色,
故答案为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡.静置后CCl4层溶液变为紫红色;
(4)为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论,
故答案为:确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰;
(5)因同一主族元素,从上到下,电子层数依次增多,原子半径逐渐增大,元素的金属性逐渐增强,原子核对最外层电子的引力逐渐减弱,
故答案为:原子半径逐渐增大(或电子层数逐渐增加).
点评 本题主要考查了卤素单质间的置换反应,题目难度中等,注意掌握卤素单质的性质及递变规律,试题侧重基础知识的考查,培养了学生灵活应用基础知识的能力和化学实验能力.


科目:高中化学 来源: 题型:多选题
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | NO3-、K+、Cl-、Na+ | D. | K+、Cl-、Al3+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应的本质是有化合价的升降 | |
| B. | 据丁达尔效应可将分散系分为溶液、胶体与浊液 | |
| C. | 向醋酸溶液中加入少量氢氧化钠溶液,由于发生中和反应,溶液的导电能力降低 | |
| D. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第二位 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
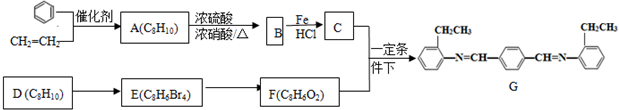

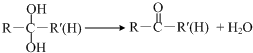
 +CH2=CH2$\stackrel{催化剂}{→}$
+CH2=CH2$\stackrel{催化剂}{→}$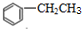 .
.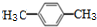 +4Br2$\stackrel{催化剂}{→}$
+4Br2$\stackrel{催化剂}{→}$ 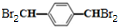 +4HBr.
+4HBr.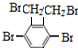 、
、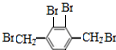 、
、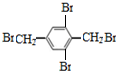 等(仅写3种).
等(仅写3种).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素编号 | 元素特征信息 |
| A | A的单质是密度最小的物质 |
| B | B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D与B同周期,该周期中D的简单离子半径最小 |
| E | B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F | F元素最高正价与最低负价的代数和为4 |
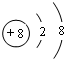 .
.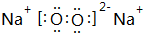 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com