
| 选项 | A | B | C | D |
| n(CO2)/mol | 2 | 3 | 4 | 5 |
| n(沉淀)/mol | 2 | 2 | 3 | 2 |
| A. | A | B. | B | C. | C | D. | D |
分析 CO2通入到NaOH、Ba(OH)2、NaAlO2的混合溶液,反应的先后顺序依次为:CO2+Ba(OH)2=BaCO3↓+H2O、2NaOH+CO2=Na2CO3+H2O、2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3,若二氧化碳过量,还发生:Na2CO3+CO2+H2O=2NaHCO3、BaCO3+CO2+H2O=Ba(HCO3)2,根据反应的方程式计算.
解答 解:A.通入2mol二氧化碳,先发生反应:Ba(OH)2+CO2=BaCO3↓+H2O,消耗1mol二氧化碳,生成1mol碳酸钡沉淀,由CO2+2NaOH=Na2CO3+H2O,剩余的1mol二氧化碳与2mol氢氧化钠反应恰好反应,则沉淀只有1mol,故A错误;
B.当通入的n(CO2)=3 mol时,
Ba(OH)2+CO2=BaCO3↓+H2O
1mol 1mol 1mol
2NaOH+CO2=Na2CO3+H2O
2mol 1mol
2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3,
2mol (3-1-1)mol 2mol
所以产生的沉淀是BaCO3和Al(OH)3且n(沉淀)之和是3mol(1mol BaCO3和2mol Al(OH)3),故B错误;
C.通入4mol二氧化碳,先发生反应:Ba(OH)2+CO2=BaCO3↓+H2O,消耗1mol二氧化碳,生成1mol碳酸钡沉淀,剩余3mol二氧化碳与氢氧化钠发生反应:CO2+NaOH=NaHCO3,消耗二氧化碳2mol,最后1mol二氧化碳与Na[Al(OH)4]发生反应2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3,生成2mol氢氧化铝沉淀,故生成沉淀总物质的量为3mol,故C正确;
D.当通入5mol二氧化碳,分别发生反应Ba(OH)2+CO2=BaCO3↓+H2O,CO2+NaOH=NaHCO3,2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3,生成1mol碳酸钡、2mol氢氧化铝沉淀,2mol碳酸氢钠,1mol碳酸钠,消耗4mol二氧化碳,剩余的1mol二氧化碳分别与生成的1mol碳酸钠发生反应:Na2CO3+CO2+H2O=2NaHCO3 ,所以沉淀的物质的量为3mol,故D错误,
故选C.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的先后顺序及反应原理为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 用湿润的蓝色石蕊试纸检验氨气 | |
| B. | 蒸馏实验中,温度计水银球应位于蒸馏烧瓶支管口处 | |
| C. | 只用BaCl2溶液就可以鉴别SO42-和CO32- | |
| D. | 可用酒精萃取碘水中的碘单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①②④ | C. | ①③④ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨作电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+ | |
| B. | 碳酸钠溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-═Fe3+ | |
| D. | NaHSO4在水溶液中电离:NaHSO4=Na++HSO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | ||
| Y | Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
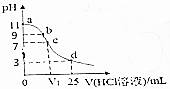
| A. | MOH电离方程式为:MOH═M++OH- | |
| B. | 在b点,离子浓度大小为c(OH-)>c(H+)>c(M+)>c(Cl-) | |
| C. | 在c点,滴加的V(HCl)>12.5mL | |
| D. | 在d点,c(Cl-)=2c(MOH)+2c(M+)=0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
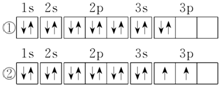
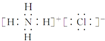 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com