

���� ��1����NO��g��+O3��g���TNO2��g��+O2��g����H=-200.9kJ•mol-1
��NO��g��+$\frac{1}{2}$O2��g���TNO2��g����H=-58.2kJ•mol-1
�ɸ�˹���ɣ���+2���ڿɵã�3NO��g��+O3��g���T3NO2��g������H������Ӧ�ļ��㣻
��2���ٷ�Ӧ���Է����У�˵����H-T��S��0������ӦΪ�������ʵ�����С�ķ�Ӧ�����Ҷȼ�С�����÷�Ӧ�ġ�S��0��
���ȼ���ƽ��ʱ������Ũ�ȣ��ٴ���K=$\frac{c��{N}_{2}{O}_{5}����c��{O}_{2}��}{{c}^{2}��N{O}_{2}����c��{O}_{3}��}$����ƽ�ⳣ����
��A��NO2��ƽ����Ӧ����v��NO2��=$\frac{��v��N{O}_{2}��}{��t}$��
B�������ʱ��Ũ����Qc����ƽ�ⳣ��K�Ƚ��жϷ�Ӧ���з������жϷ�Ӧ�ﵽƽ��ǰv��������v���棩��Դ�С��
C������NO2��Ũ�ȱ仯�жϸı��¶�ƽ���ƶ����������¶�ƽ�������ȷ�Ӧ�����ƶ��������¶�ƽ������ȷ�Ӧ�����ƶ���
D�����ݶ���������ת���ʼ���ƽ��ʱ��������ʵ������ٽ��ƽ�ⳣ���������������
�ܶ�����������ʼŨ�Ȳ���Ϊ1mol/L������ƽ��ʱN2O5��g����Ũ�ȿ��Լ���15minƽ��ʱ����������Ũ�ȣ��ݴ���ͼ��
��3����O3����ǿ�����ԣ���������NO2��
��O3����SO2�ķ�Ӧ��������Ӱ�죬�����Ƿ�Ӧ��������
��4����Ӧǰ����������������仯��������ѹǿƽ�������������С�ķ����ƶ���Ӧ�Ǽ�ѹ��������ת��Ϊ�����壮
��� �⣺��1����NO��g��+O3��g���TNO2��g��+O2��g����H=-200.9kJ•mol-1
��NO��g��+$\frac{1}{2}$O2��g���TNO2��g����H=-58.2kJ•mol-1
�ɸ�˹���ɣ���+2���ڿɵã�3NO��g��+O3��g���T3NO2��g�������H=��-200.9kJ•mol-1��+2��-58.2kJ•mol-1��=-317.3kJ/mol��
�ʴ�Ϊ��-317.3��
��2��������ӦΪ�������ʵ�����С�ķ�Ӧ�����Ҷȼ�С�����÷�Ӧ�ġ�S��0�����ڷ�Ӧ���Է����У�˵����H-T��S��0������֪��H��0��
�ʴ�Ϊ����������
�������Ϊ2L�ĺ����ܱ������г���1mol
O3����ʼŨ��Ϊ$\frac{1mol}{2L}$=0.5mol/L��NO2����ʼŨ��Ϊ$\frac{2mol}{2L}$=1mol/L����25���ӷ�Ӧ��ƽ�⣬���ƽ��ʱN2O5��g����Ũ��Ϊ0.25mol•L-1����
2NO2��g��+O3��g��?N2O5��g��+O2��g��
��ʼŨ�ȣ�mol/L����1 0.5 0 0
�仯Ũ�ȣ�mol/L����0.5 0.25 0.25 0.25
ƽ��Ũ�ȣ�mol/L����0.5 0.25 0.25 0.25
��ƽ�ⳣ��K=$\frac{c��{N}_{2}{O}_{5}����c��{O}_{2}��}{{c}^{2}��N{O}_{2}����c��{O}_{3}��}$=$\frac{0.25��0.25}{0��{5}^{2}��0.25}$=1��
�ʴ�Ϊ��1��
��A��NO2��ƽ����Ӧ����v��NO2��=$\frac{��v��N{O}_{2}��}{��t}$=$\frac{0.5mol/L}{25min}$=0.02mol•L-1•min-1����A����
B����ʱ��Ũ����Qc=$\frac{\frac{1}{2}��\frac{1}{2}}{��\frac{2}{2}��^{2}��\frac{1}{2}}$=0.5��k=1����Ӧ������Ӧ���н���ƽ�⣬�ʷ�Ӧ�ﵽƽ��ǰv��������v���棩����B����
C��T2Kƽ��ʱNO2��Ũ��Ϊ0.60mol•L-1������T1Kƽ��ʱNO2��Ũ�ȣ�0.50mol•L-1����˵���ı��¶�ƽ�����淴Ӧ�����ƶ�������ӦΪ���ȷ�Ӧ�����¶�T2��T1����C��ȷ��
D��ά��T1Kѹ������ʹNO2ת����Ϊ60%����NO2�����ʵ����仯Ϊ2mol��60%=1.2mol����
2NO2��g��+O3��g��?N2O5��g��+O2��g��
��ʼ����mol����2 1 0 0
�仯����mol����1.2 0.6 0.6 0.6
ƽ������mol����0.8 0.4 0.6 0.6
�����������ΪVL����$\frac{\frac{0.6}{V}��\frac{0.6}{V}}{��\frac{0.8}{V}��^{2}��\frac{0.4}{V}}$=1�����V=0.71����D��ȷ��
��ѡ��CD��
�ܶ�����������ʼŨ�Ȳ���Ϊ1mol/L��15minƽ��ʱ����������Ũ��Ϊ1mol/L-2��0.2mol/L=0.6mol/L����T2K�´�0��25����c��NO2����ʱ��仯ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
��3����O3����ǿ�����ԣ����Խ�NO2�����ɸ��۵��������������N2O5������Ӧ��NO2�����ʵ������٣�
�ʴ�Ϊ��O3��NO2�����ɸ��۵��������������N2O5����
��O3����SO2�ķ�Ӧ��������Ӱ�죬�����Ƿ�Ӧ��������
�ʴ�Ϊ��SO2��O3�ķ�Ӧ��������
��4����ѹ����ʹSO3תΪ���������ƽ�������з��룬�Ӷ�ʹƽ�����������ʵ�����С�ķ����ƶ������SO2��ת���ʣ�
�ʴ�Ϊ����ѹ����ʹSO3תΪ���������ƽ�������з��룬�Ӷ�ʹƽ�����������ʵ�����С�ķ����ƶ���
���� ���⿼�黯ѧƽ����㡢��������Ի�ѧƽ���ƶ�Ӱ�졢��˹���ɵ�֪ʶ�㣬���ؿ���ѧ���������жϼ������������ѵ���ͼ�����������ʽ�����Ӧ�ã���Ŀ�ѵ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������ ��� ѡ�� | ������ | ����� | ����� | �ǵ���� |
| A | �մ� | �������� | CaCO3 | �ɱ� |
| B | ��� | Ư�� | NH3•H20 | Fe |
| C | ���� | ���Ͻ� | ʯī | ���� |
| D | ���� | CuSO4•5H2O | Na2SO4 | �ƾ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������� | c��H2O��/mol/L | c��CO��/mol/L | c��H2��/mol/L | V����V���Ƚ� |
| �� | 0.06 | 0.60 | 0.10 | V��=V�� |
| �� | 0.06 | 0.50 | 0.40 | �� |
| �� | 0.12 | 0.40 | 0.80 | V����V�� |
| �� | 0.12 | 0.30 | �� | V��=V�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| ���� | HNO2 | HClO | H2CO3 | H2SO3 |
| ����ƽ�ⳣ�� ��25�棩 | Ki=5.1��10-4 | Ki=2.98��10-8 | $\begin{array}{l}{K_{i1}}=4.3��{10^{-7}}\\{K_{i2}}=5.6��{10^{-11}}\end{array}$ | $\begin{array}{l}{K_{i1}}=1.54��{10^{-2}}\\{K_{i2}}=1.02��{10^{-7}}\end{array}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ��ʼ���ʵ��� | �� | �� | �� |
| n��H2O��/mol | 0.10 | 0.20 | 0.20 |
| n��CO��/mol | 0.10 | 0.10 | 0.20 |
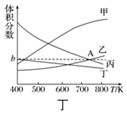
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C3H6��C5H10 | B�� | �ڶ��ױ���Զ��ױ� | ||
| C�� | C2H6��C5H12 | D�� | ��������1��2-�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com