
����Ŀ���������õ���ͨ���Ũ��NaOH��H2O2�Ļ��Һ�У��ڵ��ܿ�����Һ�ĽӴ�������˸�ĺ����֣�������Ϊͨ������Һ�в�����ClO����H2O2��ԭ���������ҷ�Ӧ�����������ϸߵ������ӣ�Ȼ������ת��Ϊ��ͨ�����ӣ�����������Ժ��ų�����ʵ�����õ�������������ͼ1��ʾ�� 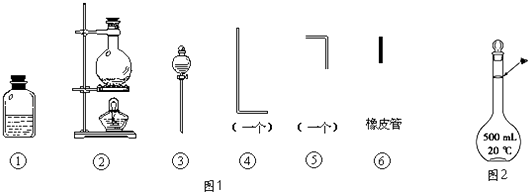
����Ҫ����д���пհף�
��1����װ��������װ��ʱ��Ӧѡ�õ�����������Ϊ����дͼ�б�ţ���
��2����ʵ�����ʱ����������������ҵ�˳�����������ĸ����������ܵı������Ϊ ��
��3�������ٵ���Ƥ��������Ӧ��2����ԭ���� ��
��4����ʵ��������10molL��1��NaOH��Һ500mL���õ�����������������ƽ���ձ��⣬�����õ��������������������ƣ�������ʱ������ͼ2����������ҺŨ�����ƫ�ߡ���ƫ�͡�����
��5��ʵ��ʱ��������ClO����H2O2��Ӧ�����ӷ���ʽΪ ��
���𰸡�
��1���ۢڢ�
��2���ڢݢޢܢ�
��3��ʹƿ����ѹǿ���
��4��500mL����ƿ������������ͷ�ιܣ�ƫ��
��5��ClO��+H2O2=Cl��+O2��+H2O
���������⣺��1�����ڷ�Ӧ���Ƕ������̺�Ũ���ᣬ�����ڷ�Ӧǰ���߲��ܻ�ϣ��÷�Һ©����װŨ���ᣬ��Ҫ�ڢ�װ�ã���Ӧ�����Ǽ��ȣ���Ҫ�ڢڸ�װ�ã�����Ҫ�õ��ܵ��������������õ��ݣ�
���Դ��ǣ��ۢڢݣ���2���ڢ��еij������ǽ���������������ڢٸ�װ�õģ�������Ҫ����Ƥ�ܽ���������̵��������������������������ĸ����������ܵı�������Ǣڢݢޢܢ٣�
���Դ��ǣ��ڢݢޢܢ٣���3������ƿ�ڲ�����������ʹƿ��ѹǿ����������Ƥ���Ŀ�������ը����С����Ϊ��ʹƿ����ѹǿ��ȣ�
���Դ��ǣ�ʹƿ����ѹǿ��ȣ���4������10molL��1��NaOH��Һ500mL����������Ϊ500mL����ƿ������������ͷ�ιܣ�����ʱ����ˮ��ˮƫ�٣���Һ���ƫС����c= ![]() ��֪��Ũ��ƫ�ߣ�
��֪��Ũ��ƫ�ߣ�
���Դ��ǣ�500mL����ƿ������������ͷ�ιܣ�ƫ�ߣ���6���������������ǿ�����ԣ�˫��ˮ�л�ԭ�ԣ����Դ���������Ӻ�˫��ˮ����������ԭ��Ӧ���������ӡ�������ˮ���������ӷ���ʽΪClO��+H2O2=Cl��+O2��+H2O�����Դ��ǣ�ClO��+H2O2=Cl��+O2��+H2O��
�����㾫����������Ҫ�����������Ļ�ѧ���ʺ�������ʵ�����Ʒ������֪ʶ�㣬��Ҫ���������Ļ�ѧ���ʣ��������Ӧ�����������ɸ�̬���ǽ�����Ӧ����ˮ��Ӧ����Ӧ���뻹ԭ�����ʷ�Ӧ��ʵ�����Ʒ���MnO2+4HCl��Ũ��=MnCl2+Cl2��+2H2O������ȷ�����⣮


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ�о���ѧϰС�������ʵ����֤Fe��Cu�Ľ�����ԣ�����������������ַ��������������������й�ʵ����Ŀ��
�����������������С��ȵ���Ƭ��ͭƬ���ֱ�ͬʱ����ϡ�����ϡ�����У��۲�������ݵĿ������ݴ�ȷ�����ǵĻ�ԣ���ԭ�������ӷ���ʽΪ ��
��������������Fe��Cu���缫��Ƴ�ԭ��أ���ȷ�����ǵĻ�ԣ���������ķ����ڻ���ԭ���װ��ͼ�����ԭ��صĵ缫���Ϻ͵������Һ��
��д���缫��Ӧʽ��������Ӧʽ����������Ӧʽ����
�����������ѧ��֪ʶ���������������һ����֤Fe��Cu��Եļ�ʵ�鷽���뷽��������ͬ�� �� �����ӷ���ʽ��ʾ�䷴Ӧԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪I��II��Ӧ��һ���������ʱ估ƽ�ⳣ�����£�
2H2(g)+S2(g)![]() 2H2S(g)K 1 ��H1 ��1��
2H2S(g)K 1 ��H1 ��1��
3H2(g)+SO2(g)![]() 2H2O(g)+H2(g)K2 ��H2��2��
2H2O(g)+H2(g)K2 ��H2��2��
��1������Hl����H2��ʾ��Ӧ4H2(g)+2SO2(g)![]() S2(g)+4H2O(g)����H=________��
S2(g)+4H2O(g)����H=________��
��2���ش����з�Ӧ��1����������⣺
���¶�ΪT1����1L���������м���1.8molH2��1.2molS2��l0minʱ��Ӧ�ﵽƽ�⣮��ʱ���l0min��V��H2S��=0.08molL-1min-l������ʱ���������г���H2��S2��H2S��0.8mol����ƽ���ƶ�����Ϊ_______�����������������������������ƶ�������
���¶�ΪT2ʱ��T2��Tl������1L����������Ҳ����1.8molH2��1.2molS2������ƽ��ʱ���S2��ת����Ϊ25%���ݴ��ж���H1________0����������������������
��3�������£���SO2��NaOH��Һ��Ӧ�ɵõ�NaHSO3��Na2SO3�ȡ�
����֪Na2SO3ˮ��Һ�Լ��ԣ�ԭ����________��д����Ҫ��Ӧ�����ӷ���ʽ��������Һ�У�[Na+]________2[SO32-]+[HSO3-]����������������������=��������
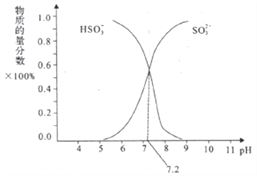
����ijNaHSO3��Na2SO3�����Һ��HSO3-��SO32-���ʵ���������pH�仯������ͼ��ʾ�����֣�������ͼʾ����SO32-��ˮ��ƽ�ⳣ��=________molL-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C�ǵ��ʣ�����A�ǽ������������ʼ��ת����ϵ��ͼ��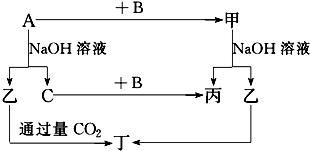
����ͼʾת����ϵ�ش�
��1��д���������ʵĻ�ѧʽ���� �� A �� C ��
��2��д�����б仯�Ļ�ѧ����ʽ������NaOH��Һ��Ӧ�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��R��X��T��Z��Q��Ԫ�����ڱ��е����λ����ͼ��ʾ������R�����ڰ�����H2���һ��ϲ�������ը���������ж���ȷ���ǣ� �� 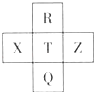
A.�ǽ����ԣ�Z��T��X
B.R��Qԭ�Ӻ�����������26
C.��̬�⻯���ȶ��ԣ�R��T��Q
D.����������ˮ��������ԣ�X��T
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ౣ�����ȵ㣬������Ҫ����һ������Ԫ�ء����ڸ��������ԭ�ӵıȽ���ȷ���ǣ� ��
A. ����Ca2+��Ca��B. �뾶Ca2+��Ca��
C. ����Ca2+��Ca��D. ����Ca2+��Ca��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ�����ֻ�����Ӧ���͵Ĺ�ϵ��ͼ��ʾ�����л�ѧ��Ӧ�в���������3�Ļ�ѧ��Ӧ�ǣ� �� 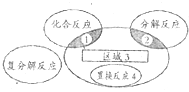
A.Br2+SO2+2H2O�TH2SO4+2HBr
B.CuO+CO ![]() Cu+CO2
Cu+CO2
C.4NH3+5O2�T4NO+6H2O
D.3Fe+4H2O��g�� ![]() Fe3O4+4H2
Fe3O4+4H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�羰������Ϊ��Ȼ���ɣ���ԭ���ǿ����е����ɵ��Ӹ����ڷ��ӻ�ԭ�����γɿ��������ӣ�����Ϊ������ά���ء������й���1mol O2����˵����ȷ���� �� ��
A. Ħ������Ϊ64g B. ��16 mol����
C. ����1 mol���� D. �������8mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp��4��10��10������˵������ȷ����

A. ��t��ʱ��AgBr��KspΪ4.9��10��13
B. ��AgBr������Һ�м���NaBr���壬��ʹ��Һ��c�㵽b��
C. ͼ��a���Ӧ����AgBr�IJ�������Һ
D. ��t��ʱ��AgCl(s)��Br��(aq)![]() AgBr(s)��Cl��(aq)ƽ�ⳣ��K��816
AgBr(s)��Cl��(aq)ƽ�ⳣ��K��816
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com