
25℃时,在10mL浓度均为0.1mol/LNaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O)
B.加入10mL盐酸时:c(NH4+) +c(H+) = c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
 D.加入20mL盐酸时:c(Cl-) =c(NH4+) +c(Na+)
D.加入20mL盐酸时:c(Cl-) =c(NH4+) +c(Na+)
【答案】B
【解析】A、混合溶液中,氢氧化钠和一水合氨的混合比例未知,故无法判断c(Na+)= c(NH3·H2O),故A错
误;B、加入10mL盐酸时,c(Cl-)=c(Na+),又根据电荷守恒得到:c(NH4+) +c(H+) + c(Na+)=c(OH
-)+c(Cl-),所以c(NH4+) +c(H+) = c(OH-),B正确;C、根据电荷守恒得到:c(NH4+) +c(H+) + c(Na+)
= c(OH-)+c(Cl-),pH=7时,即c(H+) = c(OH-),所以c(NH4+) + c(Na+)= c(Cl-),c(Cl-) >c(Na
+),故C错误;D、加入20mL盐酸时, c(Cl-)=2 c(Na+),由于铵根离子的水解,c(NH4+) ﹤c(Na+),
所以c(Cl-)>c(NH4+) +c(Na+),故D错误,此题选B。
【考点定位】本题重点考查溶液中水的电离和离子的水解,比较溶液中离子浓度的大小,物料守恒,电荷守恒和质子守恒原理的应用。
【名师点睛】溶液中离子浓度大小比较,是全国高考的热点题型之一,重复率达100%,因为这类题目涉及的知
识点多,难度大,区分度高。解决这类题目必须掌握的知识基础有:掌握强弱电解质判断及其电离,盐类的
水解,化学平衡理论(电离平衡、水解平衡),电离与水解的竞争反应,以及化学反应类型,化学计算,甚至还要
用到"守恒"来求解。解题的关键是运用物料守恒、电荷守恒和质子守恒原理计算相关离子浓度大小。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
L、M、R、T、W是原子序数依次增大的短周期主族元素,M、T在周期表中的相对位置如右表;L与R原子的最外层电子数相同,R的单质是一种常见的半导体材料。请回答下列问题:
| M | |
| T |
(1)T原子的结构示意图为________,元素W在周期表中位于第____________族,M单质分子的电子式为________。
(2)R是组成玻璃的元素之一,不能用带磨口玻璃塞的试剂瓶盛放氢氧化钠溶液的原因是(用化学方程式表示)________________________________________ _______________
________________________________________________________________________。
(3)下列有关相应元素非金属性强弱比较的说法,正确的是(填序号)________。
a.M的气态氢化物比R的气态氢化物稳定,则非金属性M强于R
b.高温下,L的单质能从R的最高价氧化物中置换出R,则非金属性L强于R
c.W的核电荷数比T多,原子半径比T小,得电子能力强,则非金属性W强于T
d.同温、同物质的量浓度的Na2LO3和Na2TO4溶液的pH:Na2LO3>Na2TO4,则非金属性T强于L
(4)工业上可用二氧化硅、氯气和焦炭在高温条件下制备RW4,该反应中除RW4外的另一种产物可用于工业炼铁。制备RW4的化学方程式为__________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物M是一种治疗心脏病的中间体,以A为原料的工业合成路线如下图所示:
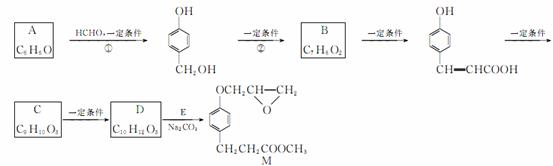
已知:RONa+R′Cl→ROR′+NaCl。
根据题意完成下列填空:
(1)写出反应类型:反应①____________;反应②____________。
(2)写出结构简式:A__________________________;
C__________________________。
(3)写出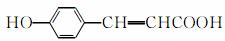 的邻位异构体分子内脱水生成香豆素的结构简式:
的邻位异构体分子内脱水生成香豆素的结构简式:
________________________________________________________________________。
(4)由C生成D的另一个反应物是________,反应条件是
____________________________ _
_ ___________________________________________。
___________________________________________。
(5)写出由D生成M的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(6)A也是制备环己醇(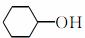 )的原料,写出检验A已完全转化为环己醇的方法。
)的原料,写出检验A已完全转化为环己醇的方法。
________________________________________________________________________
_____________________________________________________ ___________________。
___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,加入2molA和1molB发生如下反应:2A(g)+B(?) 2C(g)+D(g),
2C(g)+D(g),
C的体积分数(C%) 随时间的变化趋势符合下图关系:
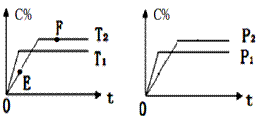
下列说法正确的是
A.E点的v(逆)大于F点的v(正)
B.若给容器加热,该反应的平衡常数K将增大
C.若在F点时给容器加压,达新平衡时C的浓度将增大
D.在恒温恒容下达平衡后,向容器中再加入2molA和1molB,A的转化率将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B.25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7
C.25℃时,0.1mol·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
D.0.1 mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023
B.室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7
C.钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀
D.一定条件下反应N2+3H2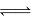 2NH3达到平衡时,3v正(H2)=2v逆(NH3)
2NH3达到平衡时,3v正(H2)=2v逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为____________。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中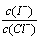 为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) ===H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(4)Bodensteins研究了下列反应:
2HI(g) H2(g) + I2(g)
H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
① 根据上述实验结果,该反应的平衡常数K的计算式为:___________。
② 上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=__________min-1
③ 由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重 新达到平衡,相应的点分别为_________________(填字母)
新达到平衡,相应的点分别为_________________(填字母)

查看答案和解析>>
科目:高中化学 来源: 题型:
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)原子序数为29的铜元素位于元素周期表中第 周期。
(2)某青铜器中Sn、Pb的质量分别为119g、20.7g,则该青铜器中Sn和Pb原子的数目之比为 。
(3)研究发现,腐蚀严重的青铜器表面大都存在CuCl。关于CuCl在青铜器腐蚀过程中的催化作用,下列叙述正确的是 。
A.降低了反应的活化能 B.增大了反应的速率
C.降低了反应的焓变 D.增大了反应的平衡常数
(4)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分CuCl发生复分解反应,该化学方程式为 。
(5)题11图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
①腐蚀过程中,负极是 (填图中字母“a”或“b”或“c”);
②环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈u2(OH)3Cl,其离子方程式为 ;
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为 L(标准状况)。

查看答案和解析>>
科目:高中化学 来源: 题型:
一定质量的无水乙醇完全燃烧时放出的热量为Q,它所生成的CO2用过量饱和石灰水完全吸收,可得100 g CaCO3沉淀,则在此条件下完全燃烧1 mol无水乙醇时放出的热量是
( )
A.0.5Q B.Q C.2Q D.5Q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com