
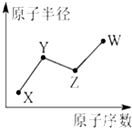
 U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随
U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随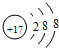 ;
;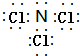 ;
;分析 Y的最高价氧化物对应的水化物可与其简单氢化物反应可生成离子型晶体的一种盐,则Y为N元素;Z是地壳中含量最多的元素,则Z是O元素;W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N,且原子半径小于N,故X为H元素;U原子最外层电子数是次外层电子数的两倍,原子只能有2个电子层,最外层电子数为4,故U为C元素;V为原子核内有12个中子的二价金属,令其相对分子质量为a,根据电子转移守恒,则:$\frac{2.4}{a}$×2=$\frac{2.24}{22.4}$×2,解得=24,则V的质子数为24-12=12,故V为Mg.
解答 解:Y的最高价氧化物对应的水化物可与其简单氢化物反应可生成离子型晶体的一种盐,则Y为N元素;Z是地壳中含量最多的元素,则Z是O元素;W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N,且原子半径小于N,故X为H元素;U原子最外层电子数是次外层电子数的两倍,原子只能有2个电子层,最外层电子数为4,故U为C元素;V为原子核内有12个中子的二价金属,令其相对分子质量为a,根据电子转移守恒,则:$\frac{2.4}{a}$×2=$\frac{2.24}{22.4}$×2,解得=24,则V的质子数为24-12=12,故V为Mg,
(1)Y为N元素,在周期表中的位置:第二周期ⅤA族,故答案为:第二周期ⅤA族;
(2)W的简单离子为Cl-,Cl-的结构示意图为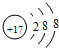 ,故答案为:
,故答案为: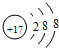 ;
;
(3)氢化物稳定性与元素非金属性一致,非金属性F>Cl>S,故氢化物稳定性:HF>HCl>H2S,故答案为:HF>HCl>H2S;
(4)由W、Y两种元素组成的一种化合物,每个原子最外层均达到8电子稳定结构,该化合物为NCl3,该化合物的电子式为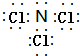 ,故答案为:
,故答案为: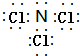 ;
;
(5)UZ2为CO2,结构式为O=C=O,故答案为:O=C=O;
(6)由X、Y、Z三种元素组成的化合物,是一种常见的化肥,其原子个数比为4:2:3,该物质为NH4NO3,含有离子键、共价键,故答案为:离子键、共价键;
(7)V与W两元素最高价氧化物的水化物分别为Mg(OH)2、HClO4,二者反应的离子方程式:Mg(OH)2+2H+=Mg2++2H2O,故答案为:Mg(OH)2+2H+=Mg2++2H2O.
点评 本题考查位置结构性质关系等,难度中等,推断元素是解题的关键,注意对元素周期律的理解与运用,熟练掌握元素化合物知识.


科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
 ,元素Y在周期表中的位置是第二周期VA族.
,元素Y在周期表中的位置是第二周期VA族.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y) | |
| B. | Y、W最高价氧化物对应水化物均能溶解Z的氢氧化物 | |
| C. | 元素W的简单气态氢化物的热稳定性比X的强 | |
| D. | 元素X、Y只能形成一种化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol碳正离子CH5+所含的电子数为11NA | |
| B. | 标准状况下,22.4L辛烷完全燃烧后生成二氧化碳分子数为8NA | |
| C. | 0.5mol乙烷分子中含共价键3.5NA | |
| D. | 乙烷可以发生氧化反应和取代反应.30g乙烷完全燃烧消耗3.5mol氧气,与氯气反应生成C2H4Cl2时,一定为纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成 气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极生成 气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
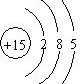 .
.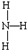 .X在纯氧中燃烧的产物无毒无污染,该反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
.X在纯氧中燃烧的产物无毒无污染,该反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据金属失去电子的多少来判断,失去电子较多的金属性较强 | |
| B. | 用钠置换MgCl2溶液中的Mg2+,来验证钠的金属性强于Mg | |
| C. | Mg不与NaOH溶液反应而Al能与NaOH溶液反应,可说明金属性:Al>Mg | |
| D. | 碱性:NaOH>Mg(OH)2>Al(OH)3,可说明钠、镁、铝金属性依次减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com