
现有KCl和KBr的混合物3.87 g,将混合物全部溶于水,并加入过量的AgNO3溶液,充分反应后产生6.63 g沉淀物,则原混合物中钾元素的质量分数为
A.24.1% B.25.9% C.40.3% D.48.1%
科目:高中化学 来源:2015-2016学年云南省高一上学期10月月考化学试卷(解析版) 题型:选择题
下列说法中,正确的是
A.分离酒精和CCl4的混合物,可用过滤法
B.从Na2CO3溶液中得到Na2CO3,可用分液法
C.从I2的CCl4溶液中得到CCl4,可用蒸馏法
D.分离NaCl和AgCl的混合物,可用萃取法
查看答案和解析>>
科目:高中化学 来源:2016届广东省高三上学期12月月考理综化学试卷(解析版) 题型:填空题
燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)污染也跟冬季燃煤密切相关。SO2、CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)光气 (COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)
 COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中固定体积容器内各物质的浓度随时间变化的曲线。回答下列问题:
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中固定体积容器内各物质的浓度随时间变化的曲线。回答下列问题:

① 0~6 min内,反应的平均速率v(Cl2)= ;
②下列说法不能判断该反应达到化学平衡状态的是 。(填字母)
A.体系中Cl2的转化率不变
B.体系中气体的平均摩尔质量不再改变
C.每消耗1mol CO的同时生成1mol COCl2
D.混合气体密度不变
③随温度升高,该反应平衡常数变化的趋势是 ;(填“增大”、“减小”或“不变”)
④比较第8 min反应温度T(8)与第15 min反应温度T(15)的高低:T(8) T(15)
(填“<”、“>”或“=”)。
⑤若保持温度不变,在第7 min 向体系中加入这三种物质各2 mol,则平衡
移动(填“向正反应方向”、“向逆反应方向”或“不”);
(2)有一种用CO2生产甲醇燃料的方法:CO2+3H2 CH3OH+H2O
CH3OH+H2O
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-b kJ·mol-1;
H2O(g)=H2O(l)△H=-c kJ·mol-1;
CH3OH(g)=CH3OH(l)△H=-d kJ·mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:____________________________;
(3)如图所示,利用电化学原理将SO2 转化为重要化工原料C

若A为SO2,B为O2,则负极的电极反应式为:________________________;
查看答案和解析>>
科目:高中化学 来源:2016届广东省、潮州金中高三上学期期中联考理综化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项 | 现象或事实 | 解释 |
A. | 浓氨水可检验氯气管道泄漏 | 浓氨水与氯气发生复分解反应 |
B. | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
C. | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与HN4Cl反应生成氨气会降低肥效 |
D. | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液中置换出铜 |
查看答案和解析>>
科目:高中化学 来源:2016届江西省新余、 万载、宜春三校高三上学期10月联考化学试卷(解析版) 题型:推断题
已知C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态,且G为黄绿色;形成D的元素原子的最外层电子数是次外层的3倍;B的焰色反应呈紫色(透过蓝色钴玻璃);K为红棕色粉末。其转化关系如图。
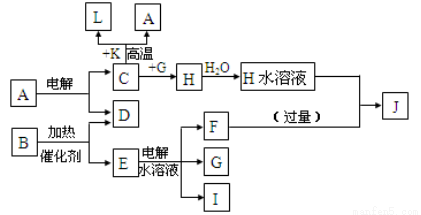
请回答:
(1)工业上制C用A不用H的原因 。
(2)写出C与K反应的化学方程式 ,该反应的反应物总能量 (填“大于”或“小于”)生成物总能量。
(3)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,接通电源(短时间)电解E水溶液的化学方程式 。
(4)写出E物质的电子式 。
(5)J与H反应的离子方程式为 。
(6)写出G与熟石灰反应制取漂白粉的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省新余、 万载、宜春三校高三上学期10月联考化学试卷(解析版) 题型:选择题
有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数之比为2:3:3,向溶液中通入氯气,使溶液中Cl-和Br-的个数比为7:3(已知还原性I->Fe2+>Br->Cl-),则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为
A.5:4 B.4:5 C.5:12 D.12:5
查看答案和解析>>
科目:高中化学 来源:2016届江西省新余、 万载、宜春三校高三上学期10月联考化学试卷(解析版) 题型:选择题
下列选项中所涉及的两个量一定相等的是
A.11.2 L Cl2与4.25 g NH3所含有的原子数
B.等质量的Al分别与足量的盐酸、NaOH溶液反应转移的电子数
C.标准状况下36 g H2O与1.204×1024个O2分子所占的体积
D.18.0 g重水(D2O)与20 g Ne所含有的电子数
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江铁人中学高一上第一阶段测化学卷(解析版) 题型:选择题
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当他们的体积比为3:2:1时,三种溶液中Cl-离子的物质的量浓度之比是
A.1:1:1 B.1:2:3 C.3:2:1 D.3:4:3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32—
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42—
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com