
����Ŀ��ij������ȤС����е��ԭ����ʵ��̽�����������µ�ʵ�飺��ͭΪ�缫������ͼ��ʾ��װ�õ�ⱥ��ʳ��ˮ��
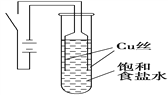
ʵ������ͨ��Դ30 s�ڣ������������ְ�ɫ���ǣ�֮���ɳȻ�ɫ���ǣ���ʱ�ⶨ��Һ��pHԼΪ10��һ��ʱ����Թܵײ��ۼ�������ɫ��������Һ��Ϊ��ɫ��
�������ϣ�
���� | �Ȼ�ͭ | ������ͭ | ��������ͭ(���ȶ�) | �Ȼ���ͭ |
��ɫ | �������ɫ��Ũ��Һ����ɫ��ϡ��Һ����ɫ | ��ɫ | �Ȼ�ɫ | ��ɫ |
�� ��ͬ�¶���CuCl���ܽ�ȴ���CuOH��
����˵��������ǣ� ��
A. ��Ӧ������������Һ�ʼ��� B. �����Ϸ����ĵ缫��ӦΪ��2H2O + 2e�� == H2��+ 2OH��
C. ���������������������� D. �Թܵײ���ɫ�Ĺ�����л�ԭ��
���𰸡�A
��������A�����������Ϣ֪��������Һ��ɳȻ�ɫ���ǣ�����������ͭ����ʱ��Һ��pHԼΪ10����Һ��ʾ���ԣ����������������Ӻ�ͭ���ӽ�����ɳ����ҷֽ⣬��˷�Ӧ��������Һ�����ԣ���A����B�����������ǵ������ˮ��������������ӵõ��ӵĻ�ԭ��Ӧ�������ĵ缫��ӦΪ��2H2O+2e-�TH2��+2OH-����B��ȷ��C���������е�����е�������������������������C��ȷ��D���Թܵײ���ɫ�Ĺ�����������ͭ�����е�CuԪ����+1�ۣ����л�ԭ�ԣ���D��ȷ����ѡA��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ˮ�г�����һ������ Cr2O72���� CrO42�������ǻ����̬ϵͳ�����ܴ���˺�����ҵ�϶Է�ˮ�����Ĺ�����������
![]()
��1��CrO4�� Cr �Ļ��ϼ� ��Cr3+�ĺ�������Ų�ʽΪ ��
��2��д�����������������ӷ�Ӧ����ʽ ���������£���Сƽ����ϵ�� pH �� pH=2������Һ�������� ɫ��
(3���������У���ԭ 0.01mol Cr2O72�����ӣ���Ҫ mol �� FeSO4��7H2O
��4����֪ Cr��OH��3 ����Һ�д�������ƽ�⣺H++CrO2-+H2O ![]() Cr��OH��3
Cr��OH��3![]() Cr3++3OH-�����й�˵������ȷ����
Cr3++3OH-�����й�˵������ȷ����
a���� HCl ��ƽ��������ƶ��������� Cr3+��
b���������ʷ��� Cr��OH��3 ������������������������
c��Cr3+������μ��� NaOH ��Һ���Ȳ����������������ʧ
d��Cr��OH��3 ������Һ��һ���� c(H )=c(OH )
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. HClO��HNO3��KMnO4���dz�����������
B. SiO2��NO2��Al2O3����������������
C. ���ʺ硢ѪҺ����±ˮ�㶹�������ڻ�ѧ�仯
D. SO3��Na2O���ױ������ڵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Cu��CuO��CuCO3��ϡH2SO4��Na2SO4��Һ���������У�ÿ�������ʷ�Ӧ������CuSO4�ķ����У� ��
A.2��
B.3��
C.4��
D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������X���߶�BaSO4�������ϲ�����ԣ�ҽѧ���ڽ�������ϵͳ��X������ʱ������BaSO4���ڷ���Ӱ�������ּ���ֶγ�Ϊ�����ӡ�
��1��ҽѧ�Ͻ��б�����ʱΪʲô����BaCO3��������________ (�����ӷ���ʽ��ʾ)��
��2��ij����С��Ϊ��̽��BaSO4���ܽ�ȣ��ֱ�����BaSO4���룺
A��5 mLˮ��
B��40 mL 0.2 molL-1��Ba(OH)2��Һ��
C��20 mL 0.5 molL-1��Na2SO4��Һ��
D��40 mL 0.1 molL-1��H2SO4��Һ�С�
���ܽ�BaSO4���γɵ���Һ�У�Ba2+|��Ũ���ɴ�С��˳��Ϊ________������ĸ����
A��b��a��c��d B��b��a��d��c C��a��d��c��b D��a��b��d��c
����֪298 Kʱ��Ksp(BaSO4)��1.1��10-10�����������£���Һb������BaSO4��c(SO42-)Ϊ__________ molL-1����Һc������BaSO4��c(Ba2+)Ϊ__________ molL-1��
�������£�������Һb����Һdֱ�ӻ�ϣ�����Һ��pHΪ__________(������Һ�����Ϊ���ǰ����Һ�����֮��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ƶ�����֣�����Ӱ�����ǵ�����ͽ�����������Ҫ��Ⱦ��Ϊ�����������PM2.5������Ҫ��ԴΪȼú��������β���ȡ���ˣ���PM2.5��SO2��NOx�Ƚ����о�������Ҫ���塣��ش��������⣺
��1����PM2.5����������ˮ�����Ƴɴ���������
����ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
Ũ��mol/L | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
���ݱ��������ж�������pH=_________��
��2������β����NOx��CO�����ɣ�
����֪����������NO�ķ�ӦΪ��N2(g)+O2(g)![]() 2NO(g) ��H>0���£������ܱ������У�����˵������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����____
2NO(g) ��H>0���£������ܱ������У�����˵������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����____
A.���������ܶȲ��ٱ仯 B.��������ƽ�����������ٱ仯
C.N2��O2��NO�����ʵ���֮��Ϊ1��1��2 D.�����İٷֺ������ٱ仯
������ȼ�Ͳ���ȫȼ��ʱ����CO���������밴���з�Ӧ��ȥCO��2CO(g)=2C(s)+O2(g)����֪�÷�Ӧ�ġ�H��0����������ܷ�ʵ��______________����ܡ����ܡ���
��3��Ϊ����SO2���ŷţ�����ȡ�Ĵ�ʩ�У�
�ٽ�úת��Ϊ�������ȼ�ϡ���֪��
H2(g)+ 1/2O2(g) =H2O(g) ��H=��241.8kJ��mol-1
C(s)+1/2O2(g) =CO(g)��H =-110.5kJ��mol-1
д����̿��ˮ������Ӧ���Ȼ�ѧ����ʽ��___________________��
��ϴ�Ӻ�SO2��������
��4������β����������Ҫԭ����2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)����H��0�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬����_________������ţ�������ͼ��v����K��n��w�ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ���������������
2CO2(g)+N2(g)����H��0�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬����_________������ţ�������ͼ��v����K��n��w�ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ���������������

�����ŷŵĵ������úȼ�ղ����Ķ��������ǵ������������ġ�������ס�֮һ������̿�ɴ���������Ⱦ��NO����5L�ܱ������м���NO�ͻ���̿�����������ʣ���һ����������������E��F�����¶ȷֱ���T1���T2��ʱ����ø�����ƽ��ʱ���ʵ�����n/mol�����±���
���� �¶�/�� | ����̿ | NO | E | F |
��ʼ | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
��1��д��NO�����̿��Ӧ�Ļ�ѧ����ʽ______________________��
��2������������ӦT1��ʱ��ƽ�ⳣ��K1=__________________����T1��T2����÷�Ӧ�ġ�H__________________0(���������������������
��3��������ӦT1��ʱ�ﵽ��ѧƽ�����ͨ��0.1molNO���壬��ﵽ�»�ѧƽ��ʱNO��ת����Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�������ȷ�Ӧ����( )��
A.�������������������ֽ�
B.������������ȼ��
C.̼��Ƹ��·ֽ�������ƺͶ�����̼
D.�������غ������к�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ,���Ƿ��ȷ�Ӧ����( )��
A.��Ƭ��ϡ����ķ�Ӧ
B.Ba(OH)2��8H2O��NH4Cl�ķ�Ӧ
C.���ȵ�̿��CO2�ķ�Ӧ
D.���ȵĽ�̿��ˮ�����ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ������ͭƬ��Ũ������ȡSO2����֤�����ʵ�װ��ͼ�����Թܢ��м���һС��ͭƬ���ټ���3~5mL Ũ���ᣬ�ô����ܵĵ������������Թܣ����ȣ������ɵ�����ͨ���Թܢ����Һ�С�

�����Թܢ��е���Һ��ʯ����Һ����Ӧһ��ʱ����Թܢ��п�����������_______________
_______________________���������ɵ�SO2����ˮ��Һ����_____�ԣ�SO2��ˮ��Ӧ�Ļ�ѧ����ʽΪ��__________________________________��
�����Թܢ��е���Һ��Ʒ����Һ����Ӧһ��ʱ�������������_____________________��˵��SO2����________�ԡ���Ӧ��ֺ�ȡ���Թܢ��ھƾ����ϼ��ȣ�������������__________________________________________________________
��ʵ������У��Թܢ�ܿ���һ�Ž���NaOH��Һ������������_______________���йط�Ӧ�����ӷ���ʽΪ�� ________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com