

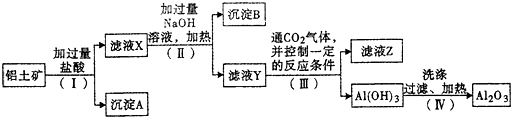
| A、图1所示装置可制取乙炔 |
| B、图2所示装置可分离乙酸乙酯和醋酸钠的水溶液 |
| C、图3所示装置可制取乙烯并验证其易被氧化 |
| D、图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
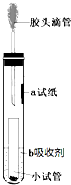 一位同学设计了一套微型装置(如图),用来完成下列实验.
一位同学设计了一套微型装置(如图),用来完成下列实验.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,由0.1mol/L一元碱BOH溶液的pH=10,可推知BOH溶液存在:BOH?B++OH- |
| B、常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D、将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池中溶液能电离出自由移动的离子 |
| B、有导线将两个活动性不同的电极连接 |
| C、正极发生了氧化反应,而负极发生了还原反应 |
| D、两电极上分别进行的氧化、还原反应中会有电子的转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH溶于水共价键被破坏 |
| B、稀有气体的原子间存在共价键 |
| C、二氧化碳分子的结构式:O═C═O |
| D、MgF2、H2O2含有的化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、振荡混合物,用分液漏斗分离 |
| B、加水振荡后,用分液漏斗分离 |
| C、加稀盐酸振荡后,用分液漏斗分离 |
| D、加入NaOH溶液后振荡,用分液漏斗分离,取下层液体通入CO2,待分层后分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向2mL 5% H2O2溶液中滴入0.1 mol/L FeCl3溶液1 mL,能较快的产生气体 |
| B、向KMnO4酸性溶液中加入过量草酸溶液,溶液紫红色褪去 |
| C、向酸性K2Cr2O7溶液中加入适量的NaOH溶液,溶液由黄色变为橙色 |
| D、向5mL 0.1mol/L Na2S2O3溶液中加入稀H2SO4,一段时间后溶液变浑浊 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com