
| |||||||||||||||||||||||||||
科目:高中化学 来源: 题型:
 硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)试剂①应选用_________(填“NaOH溶液”或“氨水”)。该试剂的用量是_________(填“过量”或“少量”)。
(2)过滤后所得沉淀①需进行洗涤,洗涤的方法是
____________________________。
(3)写出生成溶液①的离子方程式:
____________________________。
(4)以上实验设计明显存在缺陷,请将其指出
____________________________。
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 1.1水的净化与污水处理练习卷(解析版) 题型:填空题
国务院强调,调水必须坚持“三先三后”的原则。在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患。经检测,某工厂废液中含有大量的Mg2+、Al3+、Cu2+、Ag+。试分析回答下列问题。
(1)该废液中可能大量存在的一种阴离子是________(填字母代号)。
A. B.
B.
C.Cl- D.
(2)检测废液中铝元素的含量,需将其从废液样品中分离出来,所用的试剂可以是________溶液,铝元素发生变化的离子方程式是____________________________________________。
(3)为了回收废液中的金属银,某同学设计了如下方案:
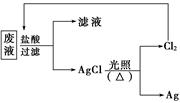
若依该方案获得Ag 108 g,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下的H2的体积为____________。(Ag的相对原子质量为108)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
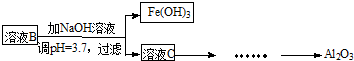 硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com