
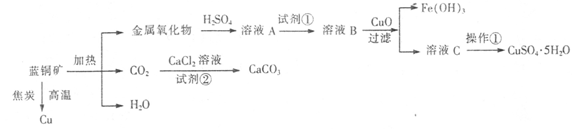
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水成分搅拌、过滤,得滤液A和沉淀B。 | |
| 步骤2: | |
| 步骤3: | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
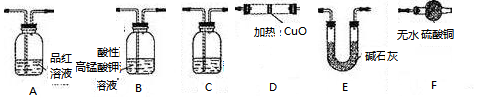
| A.① | B.②③④ | C.①②⑤ | D.③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.灼烧 | B.过滤 | C.分液 | D.蒸馏 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用加入过量氨水并过滤的方法除去NaCl溶液中混有的AlCl3 |
| B.除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤后,分液 |
| C.除去CO2中少量的HCl:气体通过盛有NaOH溶液的洗气瓶 |
| D.除去FeCl3溶液中少量的CuCl2:用足量铁粉,过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
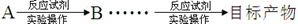 )
)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
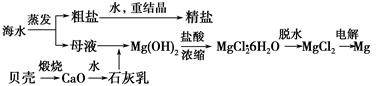
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com