
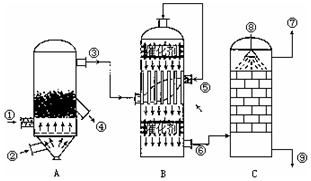
分析 根据以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图可知:
第一步:SO2的制取.主要原料是黄铁矿和空气,在高温下煅烧,使硫元素转变成SO2气体,反应方程式为:4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,设备为沸腾炉.黄铁矿需要粉碎,以增大和空气的接触面;
第二步:SO3的制取.从沸腾炉中出来的气体需经过净化、除尘,以防止催化剂中毒,进入接触室在催化剂作用下SO2和O2反应生成SO3,设备为接触室,同时涉及热量的交换、催化剂的作用、平衡的移动等问题;
第三步:硫酸的生成.从接触室中出来的气体进入吸收塔,为避免酸雾形成需用浓H2SO4吸收,以此解答(1)(2)(3)(4);
(5)二氧化硫被空气氧化为三氧化硫是可逆反应;
(6)合成氨的过程并必须选择适宜的温度,保障反应速率和限度较大;
(7)①使用催化剂,加快反应速率,缩短到达平衡的时间,平衡不移动;
②压强大,速率大,到达平衡的时间短;
③温度大,速率大,到达平衡的时间短.
解答 解:(1)煅烧黄铁矿形成的炉气主要是二氧化硫气体,另外含有杂质,能使催化剂中毒,影响催化氧化的效果;
故答案为:防止催化剂中毒;
(2)工业接触法制硫酸时,硫铁矿在沸腾炉灼烧来制取二氧化硫气体,二氧化硫和氧气在接触室中发生催化氧化来制备三氧化硫,三氧化硫在吸收塔中被98%的浓硫酸吸收制取发烟硫酸,所以涉及的设备有沸腾炉、接触室和吸收塔,故选B;
(3)进入接触室在催化剂作用下SO2和O2反应生成SO3,三氧化硫在吸收塔中被98%的浓硫酸吸收制取发烟硫酸,未反应完的SO2和O2再次进入接触室反应生成SO3,即从⑤处排出的气体是SO2和O2;
故选B;
(4)三氧化硫在吸收塔中被98%的浓硫酸吸收制取发烟硫酸,即对从进口⑧喷进的液体的98.3%的浓硫酸;
故选C;
(5)用过量的空气能促进SO2的转化,平衡正向移动,则SO2的转化率增大,
故答案为:提高SO2的转化率;
(6)合成氨的过程中,为保障反应速率和限度较大、催化剂的活性大,要选择适宜的温度400-500℃;
故答案为:提高催化剂的催化能力;
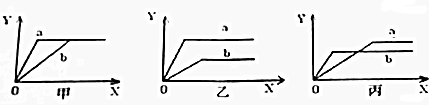
(7)①使用催化剂,加快反应速率,缩短到达平衡的时间,平衡不移动,由图可知,a先到达平衡,故a曲线表示使用催化剂,b达到平衡所用时间较长,则b曲线表示没有使用催化剂,
故答案为:a;
②由乙图可知,根据到达平衡时间,a所用时间短,说明a的反应速率快,所以a的压强高;
故答案为:a;
③由丙图可知,根据到达平衡时间,b所用时间短,说明b的反应速率快,所以b的温度高;
故答案为:b.
点评 本题考查工业制硫酸,把握制备浓硫酸的工艺流程及设备的作用、发生的化学反应为解答的关键,同时还涉及化学平衡图象、影响化学平衡的因素,试题知识点较多、综合性较强,充分考查了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 含Fe3+和NO3-,无I-和Cl- | B. | 含I-,不含Fe3+、NO3-,可能有Cl- | ||
| C. | 含NO3-,不含Fe3+、I-,可能有Cl- | D. | 含I-、Fe3+,不含Cl-,可能有NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 操作 | |
| A | 配制0.1mol•L-1氯化铝溶液 | 先将氯化铝晶体溶于浓盐酸中,后加蒸馏水稀释至指定体积 |
| B | 在加热条先下氢气还原氧化铜 | 反应完成后,先停止通入氢气,后停止加热 |
| C | 浓盐酸与碳酸钙反应制备CO2 | 气体产物先通过浓硫酸,后通过饱和碳酸氢钠溶液 |
| D | 检验某溶液是否含SO42- | 先加入BaCl2溶液,后加入盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
将溶质的质量分数为a%、物质的量浓度为c1 mol·L-1的稀硫酸加热蒸发掉一定量的水,使溶质的质量分数变为2a%,此时硫酸的物质的量浓度为c2 mol·L-1,则c1和c2的关系是( )
A.c2=2c1 B.c2>2c1 C.c2<2cl D.c1=2c2
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molH2、2molN2 | 4molH2、4molN2 | 2molNH3 |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | C3 |
| N2的体积分数 | w 1 | w 2 | w 3 |
| 混合气体的密度(g•L-1) | ?ρ1 | ?ρ2 | ?ρ3? |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
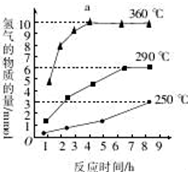 磷化氢气体(PH3)是一种强烈的储粮害虫杀剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答:
磷化氢气体(PH3)是一种强烈的储粮害虫杀剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
 H++HA-,该滚液中由水电离出的c(H+)=10-10mol/L.
H++HA-,该滚液中由水电离出的c(H+)=10-10mol/L.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com