£Ø2012?·įĢØĒųŅ»Ä££©½üÄźĄ“£¬ĪŖĢįøßÄÜŌ“ĄūÓĆĀŹ£¬Ī÷·½Ģį³ö¹²ÉśĻµĶ³£®ĢŲÖøĪŖĢįøß¾¼ĆŠ§Ņę£¬ČĖĄąÉś²ś»ī¶Æ¾”æÉÄܶą¹¦Äܻƣ®¹²Éś¹¤³Ģ½«»į“ó“ó“Ł½ų»Æѧ¹¤ŅµµÄ·¢Õ¹£®
£Ø1£©ÓÉÓŚ¹²Éś¹¤³ĢµÄÓ¦ÓĆ£¬ĄūÓĆ·¢µē³§²śÉśµÄSO
2ÖĘ³É×Ō·¢µē³Ų£¬Ęäµē³Ų·“Ó¦·½³ĢŹ½ĪŖ£ŗ2SO
2+O
2+2H
2O=2H
2SO
4£¬øƵē³Ųµē¶ÆŹĘĪŖ1.06V£®Źµ¼Ź¹ż³ĢÖŠ£¬½«SO
2ĶØČėµē³ŲµÄ
øŗ
øŗ
¼«£ØĢī”°Õż”±»ņ”°øŗ”±£©£¬øŗ¼«·“Ó¦Ź½ĪŖ
SO2+2H2O-2e-=SO42-+4H+
SO2+2H2O-2e-=SO42-+4H+
£®ÓĆÕāÖÖ·½·Ø“¦ĄķSO
2·ĻĘųµÄÓŵćŹĒ
ĄūÓĆÉĻŹöµē³Ų£¬æÉ»ŲŹÕ“óĮæÓŠŠ§ÄÜ£¬ø±²śĘ·ĪŖH2SO4£¬¼õÉŁ»·¾³ĪŪČ¾£¬ŹµĻÖ£ØÄÜÖŹ£©¹²Éś
ĄūÓĆÉĻŹöµē³Ų£¬æÉ»ŲŹÕ“óĮæÓŠŠ§ÄÜ£¬ø±²śĘ·ĪŖH2SO4£¬¼õÉŁ»·¾³ĪŪČ¾£¬ŹµĻÖ£ØÄÜÖŹ£©¹²Éś
£®
£Ø2£©ŅŌĮņĖį¹¤ŅµµÄSO
2Ī²Ęų”¢°±Ė®”¢ŹÆ»ŅŹÆ”¢½¹Ģ攢Ģ¼ĖįĒāļ§ŗĶĀČ»Æ¼ŲµČĪŖŌĮĻ£¬æÉŅŌŗĻ³ÉÓŠÖŲŅŖÓ¦ÓĆ¼ŪÖµµÄĮņ»ÆøĘ”¢ĮņĖį¼Ų”¢ŃĒĮņĖįļ§µČĪļÖŹ£®ŗĻ³ÉĀ·ĻßČēĶ¼£ŗ
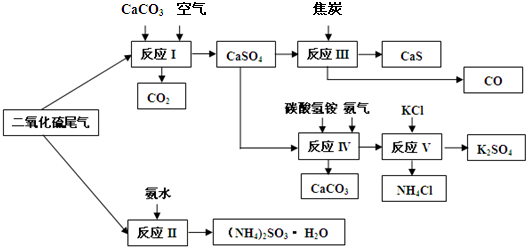
¢ŁÉś²śÖŠ£¬Ļņ·“Ó¦IIÖŠµÄČÜŅŗÖŠ¼ÓČėŹŹĮ滹ŌŠŌŗÜĒæµÄ¶Ō±½¶ž·ÓµČĪļÖŹ£¬ĘäÄæµÄŹĒ
·ĄÖ¹ŃĒĮņĖįļ§±»Ńõ»Æ
·ĄÖ¹ŃĒĮņĖįļ§±»Ńõ»Æ
£®
¢ŚĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
ABCD
ABCD
£®
A£®·“Ó¦¢ńÖŠŠč¹ÄČė×ćĮææÕĘų£¬ŅŌ±£Ö¤¶žŃõ»ÆĮņ³ä·ÖŃõ»ÆÉś³ÉĮņĖįøĘ
B£®·“Ó¦IIIÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCaSO
4+4C
CaS+4COӟ
C£®·“Ó¦IVŠčæŲÖĘŌŚ60”«70”ę£¬ÄæµÄÖ®Ņ»ŹĒ¼õÉŁĢ¼ĖįĒāļ§µÄ·Ö½ā
D£®·“Ó¦VÖŠµÄø±²śĪļĀČ»Æļ§æÉÓĆ×÷µŖ·Ź
¢Ū·“Ó¦VÖŠŃ”ÓĆĮĖ40%µÄŅŅ¶ž“¼ČÜŅŗ£¬ĪĀ¶ČæŲÖĘŌŚ25”ę£¬“ĖŹ±ĮņĖį¼ŲµÄ²śĀŹ³¬¹ż90%£¬Ń”ÓĆ40%µÄŅŅ¶ž“¼ČÜŅŗŌŅņŹĒ
K2SO4ŌŚÓŠ»śČܼĮŅŅ¶ž“¼ÖŠČܽā¶ČŠ”£¬Äܳä·ÖĪö³ö
K2SO4ŌŚÓŠ»śČܼĮŅŅ¶ž“¼ÖŠČܽā¶ČŠ”£¬Äܳä·ÖĪö³ö
£®
¢Ü£ØNH
4£©
2SO
3æÉÓĆÓŚµē³§µČŃĢµĄĘųÖŠĶѵŖ£¬½«µŖŃõ»ÆĪļ×Ŗ»ÆĪŖµŖĘų£¬Ķ¬Ź±Éś³ÉŅ»ÖÖµŖ·Ź£¬ŠĪ³É¹²ÉśĻµĶ³£®Š“³ö¶žŃõ»ÆµŖÓėŃĒĮņĖįļ§·“Ó¦µÄ»Æѧ·½³ĢŹ½
4£ØNH4£©2SO3+2NO2=4£ØNH4£©2SO4+N2
4£ØNH4£©2SO3+2NO2=4£ØNH4£©2SO4+N2
£®



 ÓŵČÉśĢāæāĻµĮŠ“š°ø
ÓŵČÉśĢāæāĻµĮŠ“š°ø
