
【题目】观察如图装置,下列说法错误的是
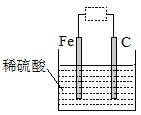
A.虚线框中接灵敏电流计,该装置可将化学能转化为电能
B.虚线框中无论是否接灵敏电流计,铁都要被腐蚀
C.虚线框中接直流电源,铁可能不易被腐蚀
D.虚线框中接灵敏电流计或接直流电源,铁都是负极
科目:高中化学 来源: 题型:
【题目】有机化学知识在生活中应用广泛。
(1)糖类、油脂和蛋白质是动物性和植物性食物中的基本营养物质。
①下列有关说法中,正确的是________________;
A.棉、麻、木材、蚕丝的主要成分都是纤维素
B.油脂是产生能量最高的营养物质
C.蛋白质在人体内发生水解最终生成氨基酸
D.糖类都是有甜味的物质
E.淀粉、纤维素、蛋白质都是天然高分子化合物
F.硫酸铵或乙酸铅溶液加入到蛋白质溶液中,蛋白质都能从溶液中析出
②葡萄糖是最重要、最简单的单糖,除了是一种营养物质,还能用在制镜等工业上。写出葡萄糖发生银镜反应的化学方程式:_____________________________________________。
(2)苹果酸常用作汽水、糖果的添加剂,其结构简式为![]() ,该分子中官能团的名称为________________,可以和醇类物质发生__________反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为_________________。
,该分子中官能团的名称为________________,可以和醇类物质发生__________反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为_________________。
(3)实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)

①在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是_____________;
②生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的有(填序号)___________________;
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的浓度不再变化
③现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。

试剂a是______,分离方法①是_______;分离方法②是________,试剂b是________;
④写出C → D 反应的化学方程式________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
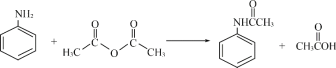
【题目】酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐或与冰醋酸加热来制取,苯胺与乙酸酐的反应速率远大于与冰醋酸反应的速率,现选用苯胺与乙酸酐为原料制取和提纯乙酰苯胺,该放热反应的原理:
密度(g/mL) | 相对分子质量 | 颜色、状态 | 溶解性 | |
苯胺 | 1.04 | 93 | 无色油状液体 | 微溶于水, 易溶于乙醇、乙醚 |
乙酸酐 | 1.08 | 102 | 无色透明液体 | 遇水缓慢反应生成乙酸 |
乙酰苯胺 | 135 | 无色片状晶体, 熔点 114℃ | 不溶于冷水,可溶于热 水、乙醇、乙醚 |
实验步骤
①取5.00mL苯胺,倒入 100mL锥形瓶中,加入20mL水,在旋摇下分批加入 6.00mL 乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至 150mL 烧杯中,加入适量水配制成 80℃的饱和溶液,再加入过量 20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸 3~5min,趁热过滤,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品。
请回答:
(1)苯胺与冰醋酸反应制备乙酰苯胺的化学反应方程式______________________。
(2)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是____________。
A.反应快结束时的充分搅拌 B.旋摇下分批加入 6.0mL 乙酸酐
C.玻璃棒将块状物研碎 D.加 20mL 水
(3)在步骤②中对粗产品进行洗涤可能需要用到以下操作:
a.加入洗涤剂至浸没固体;
b.洗涤剂缓慢通过;
c.洗涤剂快速通过;
d.关小水龙头;
e.开大水龙头;
f.重复 2~3 次。
请选出正确的操作并排序_____。(操作可重复使用)
(4)加入过量 20%的水的目的是_____。
(5)下列关于步骤③说法不正确的是__________________________。
A.活性炭吸附有色物质,可以提高产率
B.冷却时,冰水浴冷却比室温冷却更易得到大颗粒晶体便于抽滤
C.抽滤用如图装置,为防止倒吸,结束时可先关闭抽气泵,后打开活塞 a

D.洗涤完成后应将布氏漏斗从吸滤瓶上取下,左手握布氏漏斗,倒转,用右手“拍击”左手,使固体连同滤纸一起落入洁净的表面皿上,揭去滤纸,再对固体做晾干处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中蕴藏着丰富的资源。海水综合利用的流程图如下。
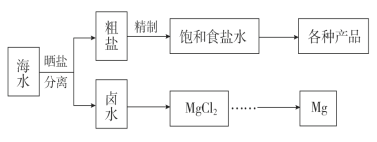
(1)用NaCl作原料可以得到多种产品。
①工业上由NaCl制备金属钠的化学方程式是______。
②写出产物氯气制备“84”消毒液的离子方程式:______。
③NaCl也是侯氏制碱法的重要反应物之一,写出侯氏制碱法过程中涉及到的两个主要方程式:__________ , __________。
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是Br2+Na2CO3+H2O―→NaBr+NaBrO3+NaHCO3,吸收1 mol Br2时,转移的电子数为________mol。
(3)海水提镁的一段工艺流程如下图:
卤水![]()
![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液→MgCl2·6H2O→MgCl2
MgCl2溶液→MgCl2·6H2O→MgCl2![]() Mg
Mg
①采用石墨电极电解熔融的氯化镁,发生反应的化学方程式_________;
②电解时,若有少量水存在,则不能得到镁单质,写出有关反应的化学方程式__________。
(4)分离出粗盐后的卤水中蕴含着丰富的镁资源,经过下列途径可获得金属镁:其中,由MgCl2·6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如下:
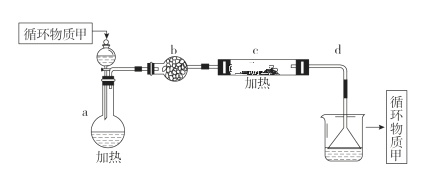
①上图中,装置a由________、________、双孔塞和导管组成。
②循环物质甲的名称是________。
③制取无水氯化镁必须在氯化氢存在的条件下进行,原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是
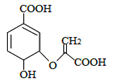
A.分子中含有2种官能团
B.可分别与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3mol NaOH发生中和反应
D.可使溴水、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制得的纯碱中往往含有少量的NaCl固体,现设计以下两种方案测定样品中纯碱的纯度。完成下列填空:
方案一:测量装置如图所示,称取样品m克装入Y型试管中。
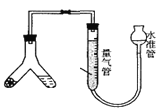
(1)检查装置气密性的方法是__________。
(2)量气管中的液体应为__________(填编号)。
a 饱和Na2CO3溶液 b 饱和NaHCO3溶液 c 饱和NaCl溶液
(3)Y型试管另一端应装入试剂为__________(填编号)。
a 盐酸 b 硫酸 c 硝酸
方案二:装置如图二所示,A中样品质量为m克。
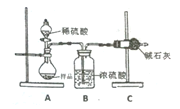
(4)根据图中所用实验装置,可以判断需要测定的实验数据是__________。
(5)仔细分析该装置,由此测的的数据计算出的实验结果有可能偏高也有可能偏低,分析原因并对装置进行相应的改进(已知:装置气密性良好);
(i)偏低的原因是____________,改进方法是__________。
(ii)偏高的原因是_____________,改进方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:
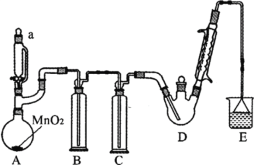
①制备反应原理:C2H5OH + 4Cl2 → CCl3CHO+5HCl
可能发生的副反应:
C2H5OH + HCl → C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 | 微溶于水,可溶于乙醇 |
(1)仪器a中盛放的试剂是_____ ;装置B的作用是__________ 。
(2)若撤去装置C,可能导致装置D中副产物________ (填化学式)的量增加;装置D可采用_________ 加热的方法以控制反应温度在70℃左右。
(3)装置E中可能发生的无机反应的离子方程式有____________________ 。
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行,为什么?_______________
(5)测定产品纯度:称取产品0.30 g配成待测溶液,加入0.1000 mol·L-1碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000 mol·L-1 Na2S2O3溶液滴定至终点。进行平行实验后,测得消耗Na2S2O3溶液20.00 mL。则产品的纯度为_________。
滴定的反应原理:CCl3CHO +OH- → CHCl3 + HCOO-、 HCOO-+ I2 =H+ + 2I- + CO2↑ I2 + 2S2O32- = 2I-+ S4O62-
(6)请设计实验证明三氯乙酸的酸性比乙酸强。 __________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池己被广泛用作便携式电源。正极材料为LiCoO2、LiFePO4等,负极材料一般为石墨碳,以溶有LiPF6、LiBF4等的碳酸二乙酯(DEC)作电解液。
(1)Fe2+基态核外电子排布式为 ________。
(2)PO43-的空间构型为 ________ (用文字描述)。
(3)![]() 中
中![]() 的配位数为6,该配合物中的配位原子为 _____。
的配位数为6,该配合物中的配位原子为 _____。
(4)碳酸二乙酯(DEC)的分子结构如图所示,分子中碳原子的轨道杂化类型为_____,1mol碳酸二乙酯(DEC)中含有σ键的数目为_____。
![]()
(5)氮化锂是一种新型无机贮氢材料,其晶胞结构如图所示,该晶体的化学式为_______。
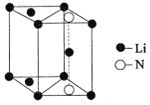
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化镁溶液的密度为1.18 g·cm-3,其中镁离子的质量分数为5.1%,该溶液中氯离子的物质的量浓度为( )
A.0.5 mol·L-1B.2 mol·L-1
C.2.5 mol·L-1D.5 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com