
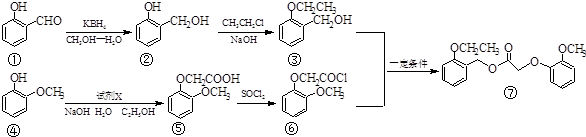
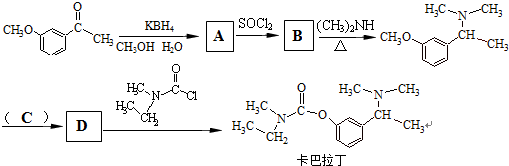
 与KBH4发生还原反应生成A为
与KBH4发生还原反应生成A为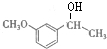 ,进而与SOCl2反应生成B为
,进而与SOCl2反应生成B为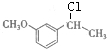 ,B发生取代反应生成
,B发生取代反应生成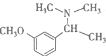 ,
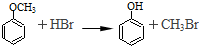
, 与HBr发生取代反应生成D为
与HBr发生取代反应生成D为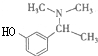 ,D发生取代反应可生成卡巴拉丁,据此解答.
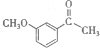
,D发生取代反应可生成卡巴拉丁,据此解答.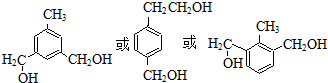 ,
, ;
;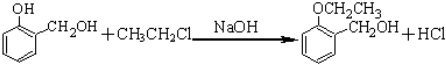 ,
,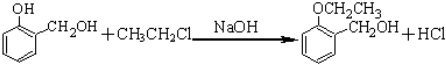 ;
; 与KBH4发生还原反应生成A为
与KBH4发生还原反应生成A为 ,进而与SOCl2反应生成B为
,进而与SOCl2反应生成B为 ,B发生取代反应生成
,B发生取代反应生成 ,
, 与HBr发生取代反应生成D为
与HBr发生取代反应生成D为 ,D发生取代反应可生成卡巴拉丁,
,D发生取代反应可生成卡巴拉丁, ;
; ;HBr;
;HBr; .
.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
| A、在非标准状况下,1 mol O2的体积也有可能是22.4 L |
| B、在温度和压强一定时,气态物质的体积主要由气体分子数目和分子的大小决定 |
| C、同温同压下,0.3 mol N2和0.7 mol O2的体积比为3:7 |
| D、同温同压下,相同体积的任何气体所含有的分子数目一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
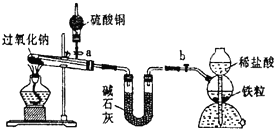 Na2O2是中学化学常用的强氧化剂,除了能与C02、H20反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验.
Na2O2是中学化学常用的强氧化剂,除了能与C02、H20反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
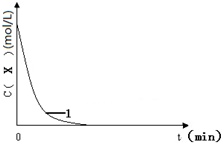 已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生.若再加入双氧水,将发生反应:H2O2+2H++2I-═2H2O+I2,且生成的I2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成的I2完全消耗.由于溶液中的I-继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝.因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I-═2H2O+I2的反应速率.
已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生.若再加入双氧水,将发生反应:H2O2+2H++2I-═2H2O+I2,且生成的I2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成的I2完全消耗.由于溶液中的I-继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝.因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I-═2H2O+I2的反应速率.| 编号 | 往烧杯中加入的试剂及其用量(mL) | 催化剂 | 开始变蓝时间(min) | ||||
| 0.1 mol?L-1 KI溶液 | H2O | 0.01 mol?L-1 X 溶液 | 0.1 mol?L-1 双氧水 | 1 mol?L-1 稀盐酸 | |||
| 1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 无 | 1.4 |
| 2 | 20.0 | m | 10.0 | 10.0 | n | 无 | 2.8 |
| 3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | 无 | 2.8 |
| 4 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5滴Fe2(SO4)3 | 0.6 |
| 气化炉中产生H2 |
| 通入水蒸气,主要化学反应: ①C(s)+H2O(g)═CO(g)+H2(g) △H=+131.6kJ mol-1 ②CO(g)+H2O(g)═CO2(g)+H2(g) △H=-41.2kJ mol-1 ③CaO(s)+CO2(g)═CaCO3(s) △H=-178.3kJ mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 现象和结论 |
| 步骤1:取少许样品于试管中,加入适量蒸馏水充分溶解,再滴加H2SO4酸化的KMnO4溶液; | 现象:若KMnO4溶液的紫红色褪为无色 ①结论:样品中有 ②褪色的离子方程式为: |
| 步骤2:另取少许样品于试管中,加入适量蒸馏水充分溶解,再滴加稀HCl,使溶液呈酸性,再滴加适量BaCl2溶液; | ③现象:若 结论:假设2成立. |
| … | … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com