
| A. | 实验室配制FeCl3溶液时,需将FeCl3 (s)溶解在较浓盐酸中,然后加水稀释 | |
| B. | 反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应△H>0,△S<0 | |
| C. | 0.1mol•L-1NH4Cl溶液加水稀释,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$的值增大 | |
| D. | 反应CH3COOCH3+H2O?CH3COOH+CH3OH△H>0,达到平衡时,加入少量固体NaOH,则乙酸甲酯水解转化率增大 |
分析 A、氯化铁直接溶于水后会发生水解;
B、G=△H-T•△S<0的反应能自发进行;
C、0.1mol•L-1NH4Cl溶液加水稀释,铵根离子的水解被促进;
D、反应CH3COOCH3+H2O?CH3COOH+CH3OH,达到平衡时,加入少量固体NaOH,则能反应掉乙酸.
解答 解:A、氯化铁直接溶于水后会发生水解,且水解显酸性,故将氯化铁固体直接溶解在盐酸溶液中,能抑制其水解,然后加水稀释至所需的浓度即可,故A正确;
B、反应2CO+2NO=N2+2CO2的气体的物质的量减小,则△S<0,而反应能自发进行,即G=△H-T•△S<0,则△H<0,故B错误;
C、0.1mol•L-1NH4Cl溶液加水稀释,铵根离子的水解被促进,则溶液中的n(H+)增多,n(NH4+)减少,故$\frac{c({H}^{+})•V}{c(N{{H}_{4}}^{+})•V}$增大,而溶液体积相同,故$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$的值增大,故C正确;
D、反应CH3COOCH3+H2O?CH3COOH+CH3OH,达到平衡时,加入少量固体NaOH,则能反应掉乙酸,导致乙酸浓度降低,则平衡右移,故乙酸甲酯的水解转化率增大,故D正确.
故选B.
点评 本题考查了盐类水解平衡的移动和盐类水解的应用,注意离子浓度的比值变化的判断方法.综合性较强,但难度不大.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 硝酸铵自发地溶于水 | |
| B. | H2O(l)═H2O(g)△H=+44.0kJ•mol-1 | |
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9 kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4 g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 常温常压下,22.4L CO2和SO2混合气体含有2NA个O原子 | |
| C. | 22.4 L CH4与18 g H2O所含有质子数均为10NA | |
| D. | 常温常压下,80g SO3含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol C3H8气体中含有共价键数目为11NA | |
| B. | 1mol Na2O和Na2O2混合物中含有的阴阳离子总数是3NA | |
| C. | 将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA个Fe3+ | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3要在沸水中才能发生水解 | |
| B. | 放热反应不需要加热就能进行 | |
| C. | 将pH=2的硫酸溶液加热至100℃时pH基本不变 | |
| D. | 加热不利于合成氨,故工业上采用低温合成氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=0.1mol/L的溶液:Na+、NH4+、SO42-、CO32- | |
| B. | 碱性溶液:Cu2+、NO3-、Fe3+、SO42- | |
| C. | 与铝粉反应放出H2的无色溶液:NO3-、Al3+、Na+、SO42- | |
| D. | 使红色石蕊试纸变蓝的溶液:SO42-、CO32-、Na+、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基丙烷(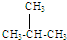 )也叫异丁烷 )也叫异丁烷 | |
| B. | 蛋白质和糖类均为天然高分子化合物 | |
| C. | 乙烯和丙烯只能发生加成反应,不能发生取代反应 | |
| D. | 苯使溴水褪色的原因是发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2(SO4)3=2Al3++3SO42- | B. | NaHCO3=Na++H++CO32- | ||
| C. | Ba(OH)2=Ba2++2 OH- | D. | Na2CO3=2Na++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨电极电解Ca(NO3)2溶液,当转移电子数为0.2 NA时,阴极析出4 g金属 | |
| B. | 0.1 mol24Mg32S晶体中所含中子总数为2.8 NA | |
| C. | 常温下含有NA个NO2、N2O4分子的混合气体,温度降至标准状况,其体积约为22.4 L | |
| D. | 在熔融状态下,1 mol NaHSO4完全电离出的阳离子数目为2 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com