
Ca(OH)2(s)
![]() Ca2++2OH-
Ca2++2OH-
在火力发电厂燃烧煤的废气中往往含有SO2、O2、N2、CO2等.为了除去有害气体SO2并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏.
(1)写出上述两个反应的化学方程式:
①SO2与CaCO3悬浊液反应:__________________________
②SO2与Ca(OH)2悬浊液反应:__________________________
(2)试说明用熟石灰的悬浊液而不用澄清石灰水洗涤废气的理由:__________________.
| 答案:(1)①2SO2+O2+2CaCO3+4H2O====2CaSO4·2H2O+2CO2
②2SO2+O2+2Ca(OH)2+2H2O====2CaSO4·2H2O (2)因为Ca(OH)2微溶于水,用澄清石灰水时,Ca(OH)2浓度低,不利于SO2的吸收
|
| 提示:石膏的化学式是CaSO4·2H2O,注意不要与生石膏2CaSO4·H2O混淆.
SO2溶于水生成H2SO3: ①H2O+SO2 但产物为CaSO4·2H2O,显然是H2SO3被氧化成了H2SO4: ②2H2SO3+O2====2H2SO4 H2SO4既可与CaCO3,又可与Ca(OH)2反应: ③H2O+CaCO3+H2SO4====CaSO4·2H2O+CO2↑ ④Ca(OH)2+H2SO4====CaSO4·2H2O 将①②③或①②④叠加可得答案.
|


科目:高中化学 来源:黄冈重点作业 高一化学(下) 题型:022
已知氢氧化钙在水中存在下列溶液平衡:Ca(OH)2(g)![]() Ca2+
+2OH- ,在火力发电厂燃烧煤的废气中往往含有
Ca2+
+2OH- ,在火力发电厂燃烧煤的废气中往往含有 、
、 、
、 、
、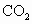 等,为了除去有害气体
等,为了除去有害气体 并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏.
并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏.
(1)写出上述两个反应的化学方程式:
① 与
与 悬浊液反应:________
悬浊液反应:________
② 与
与 悬浊液反应:________
悬浊液反应:________
(2)试说明用熟石灰的悬浊液而不用澄清石灰水洗涤废气的理由:________.
查看答案和解析>>
科目:高中化学 来源: 题型:
Ca(OH)2(s)![]() Ca2++2OH-
Ca2++2OH-
在火力发电厂燃烧煤的废气中往往含有SO2、O2、N2、CO2等。为了除去有害气体SO2并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏(CaSO4·2H2O)。
(1)写出上述两个反应的化学方程式:
①SO2与CaCO3悬浊液反应:_____________________________________________;
②SO2与Ca(OH)2悬浊液反应:____________________________________________。
(2)试说明用熟石灰的悬浊液而不用澄清石灰水洗涤废气的理由:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氢氧化钙在水中存在下列溶解平衡:Ca(OH)2(s) ≒Ca2++2OH-。在火力发电厂燃烧煤的废气中往往含有二氧化硫、氧气、氮气、二氧化碳等。为了除去有害气体二氧化硫并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏[CaSO4·2H2O]。
(1)写出上述两个反应的化学方程式:①_____________;②_________________。
(2)试说明用熟石灰的悬浊液,而不用澄清石灰水洗涤废气的理由:________。
(3)在英国进行的一个研究结果表明:高烟囱可以有效地降低地表面二氧化硫的浓度。在二十世纪六七十年代的10年间,由发电厂排放出的二氧化硫增加了35%,但由于建造高烟囱的结果使地面二氧化硫的浓度降低了30%之多。请从全球环境保护的角度,分析这种方法是否可取?答____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出上述两个反应的化学方程式:①__________________________________;
②__________________________________。
(2)试说明用熟石灰的悬浊液,而不用澄清石灰水洗涤废气的理由。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com