
| A. | FeCl3 | B. | 溴水 | C. | 石蕊试液 | D. | KMnO4溶液 |
分析 苯酚、戊烯、己烷、乙醇四种溶液分别与溴水反应的现象为:白色沉淀、溴水褪色、分层后有机层在上层、互溶无现象,以此来解答.
解答 解:A.FeCl3溶液不能鉴别戊烯、己烷,故A不选;
B.苯酚、戊烯、己烷、乙醇四种溶液分别与溴水反应的现象为:白色沉淀、溴水褪色、分层后有机层在上层、互溶无现象,现象不同可鉴别,故B选;
C.均与石蕊试液不反应,不能鉴别,故C不选;
D.苯酚、戊烯、乙醇均与KMnO4溶液反应使其褪色,不能鉴别,故D不选;
故选B.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应等为解答的关键,侧重分析与应用能力的考查,注意有机物的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
 ;
; ;
; ;
;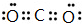 ;
;
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某白酒中的增塑剂叫邻苯二甲酸二乙酯(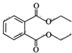 ),对人体健康有害 ),对人体健康有害 | |
| B. | 4-甲基咪唑(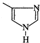 )是某饮料中检测出的致癌物,能使酸性高锰酸钾溶液褪色 )是某饮料中检测出的致癌物,能使酸性高锰酸钾溶液褪色 | |
| C. | 某媒体披露“皮革奶”事件,有不法厂商将皮革下脚料水解后掺入奶粉,以提高奶粉中蛋白质的含量.动物皮革的主要成分是蛋白质,“皮革奶”灼烧时有烧焦羽毛的气味 | |
| D. | 新西兰牛奶中检测出有毒的二氰二氨(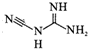 ),该物质一定不溶于水 ),该物质一定不溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
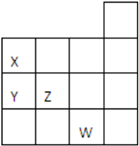 如图所示元素周期表前四周期的一部分,关于元素X、Y、Z、W的叙述不正确的是( )
如图所示元素周期表前四周期的一部分,关于元素X、Y、Z、W的叙述不正确的是( )| A. | 只有④ | B. | ①③④ | C. | ②③ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
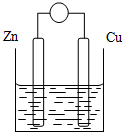 原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.
原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.| 电极 | 电极材料 | 电极反应式 | 反应类型 |
| 正极 | |||
| 负极 | |||
| 总反应式 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体氯化铵和消石灰混合加热:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+H2O | |
| B. | 硫化亚铁与盐酸反应:S2-+2H+═H2S↑ | |
| C. | 铜与稀硝酸:Cu+4H++2NO3-═Cu2++NO2↑+2H2O | |
| D. | 向氨水中通入过量的二氧化碳:NH3•H2O+CO2═NH4++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com