
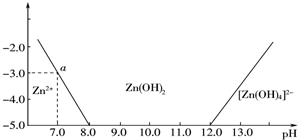
分析 (1)由图象可知溶液的碱性较强时,锌的存在形式为[Zn(OH)4]2-,结合元素守恒书写方程;
(2)根据图中数据,利用Ksp=c(Zn2+).c2(OH-)计算;
(3)pH=6时,根据Ksp求出c(Zn2+),再根据反应的锌离子的物质的量计算需要的氢氧化钠的物质的量.
解答 解:(1)由图象可知溶液的碱性较强时,锌的存在形式为[Zn(OH)4]2-,所以其反应的离子方程式为:Zn2++4OH-═[Zn(OH)4]2-;
故答案为:Zn2++4OH-═[Zn(OH)4]2-;
(2)当溶液的pH=7.0时,c(Zn2+)=10-3mol•L-1,Ksp=c(Zn2+).c2(OH-)=10-3•(10-7)2=10-17,故答案为:10-17;
(3)往1.00L 1.00mol•L-1 ZnCl2溶液中加入NaOH固体至pH=6,所以溶液中c(OH-)=10-8mol•L-1,则溶液中c(Zn2+)=$\frac{Ksp}{{c}^{2}(O{H}^{-})}$=$\frac{1{0}^{-17}}{(1{0}^{-8})^{2}}$=0.1mol/L,所以反应消耗的Zn2+的物质的量为0.9mol,所以消耗的NaOH为1.8mol,故答案为:1.8.
点评 本题考查了难溶电解质的溶解平衡,注意对图象和表格中的数据的分析,题目难度较大.


科目:高中化学 来源: 题型:解答题
 ;
; .
. 或
或 或
或 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 方法一 | CO(g)+2H2(g)?CH3OH(g) |
| 方法二 | CO2(g)+3H2(g)?CH3OH(g)+H2O(g) |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2和SO2 | B. | CO2和NH3 | C. | NO和SO2 | D. | NO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )
一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )| A. | T1>T2,该反应的△H>0 | |
| B. | 加入催化剂可以提高CO的转化率 | |
| C. | T1时的平衡常数K1>T2时的平衡常数K2 | |
| D. | CO(g)+2H2(g)?CH3OH(1)的△H值将变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2与足量的Fe充分反应,转移电子的数目为3NA | |
| B. | 常温下,1LpH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA | |
| C. | 常温下,21g乙烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 1mol${\;}_{6}^{14}$C原子中所含中子数目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗锌与稀硫酸反应比纯锌快,说明粗锌中含有更活泼的金属 | |
| B. | 新制氯水显酸性,滴加少量紫色石蕊溶液,溶液始终呈红色 | |
| C. | 常温下,弱酸酸式盐NaHA的pH=6,说明HA-的电离程度大于其水解程度 | |
| D. | 一定温度下,反应2NaCl(s)=2Na(s)+Cl2(g)的△H<0,△S>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 有一种瓦斯分析仪能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
有一种瓦斯分析仪能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )| A. | 电极a是正极,电极反应式为CH4+4O2--8e-=CO2+2H2O | |
| B. | 电极b是正极,O2-由电极b流向电极a | |
| C. | 瓦斯分析仪工作时,电池内电路中电子由电极a流向电极b | |
| D. | 当电路中有0.4mol电子转移时,a极有2.24L(标况)甲烷放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com