
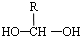
 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$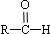 (R代表烃基).
(R代表烃基).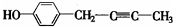 、
、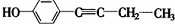 .
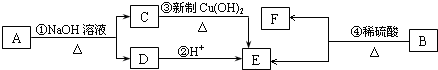
. 分析 A、B两种有机物均是有机合成的中间体,其中A的分子式为C4H7O2Br,A和氢氧化钠的水溶液发生反应生成C、D,C能和新制氢氧化铜悬浊液发生氧化反应,则C中含有醛基,D酸化得到酸,则A为含有溴原子的酯,且溴原子连接在连接醇羟基的碳原子上,C被氧化生成E,则形成A的酸、醇中碳原子个数相等,C为CH3CHO、E为CH3COOH,A为CH3COOCHBrCH3;
B分子中含2个氧原子,其燃烧产物n(CO2):n(H2O)=2:1,B中C、H原子个数之比为1:1,质谱图表明B的相对分子质量为188,设B的分子式为(CH)xO2,其相对分子质量=13x+32=188,x=12,则B的分子式为C12H12O2,B发生水解反应生成乙酸和F,根据原子守恒知F的分子式为C10H10O,不饱和度=$\frac{10×2+2-10}{2}$=6,
F具有如下特点:①遇FeCl3有显色反应,说明含有酚羟基;②核磁共振氢谱中显示五种吸收峰说明含有5种类型的H原子;③苯环上的一氯代物只有两种,说明取代位置为对位;④除苯环外,不含有其他环状结构,则F分子中应含有1个C≡C或2个C=C,则可能的结构为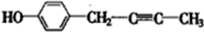 、
、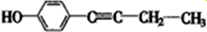 、
、 、
、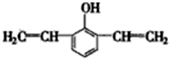 ,据此分析解答.
,据此分析解答.
解答 解:A、B两种有机物均是有机合成的中间体,其中A的分子式为C4H7O2Br,A和氢氧化钠的水溶液发生反应生成C、D,C能和新制氢氧化铜悬浊液发生氧化反应,则C中含有醛基,D酸化得到酸,则A为含有溴原子的酯,且溴原子连接在连接醇羟基的碳原子上,C被氧化生成E,则形成A的酸、醇中碳原子个数相等,C为CH3CHO、E为CH3COOH,A为CH3COOCHBrCH3;
B分子中含2个氧原子,其燃烧产物n(CO2):n(H2O)=2:1,B中C、H原子个数之比为1:1,质谱图表明B的相对分子质量为188,设B的分子式为(CH)xO2,其相对分子质量=13x+32=188,x=12,则B的分子式为C12H12O2,B发生水解反应生成乙酸和F,根据原子守恒知F的分子式为C10H10O,不饱和度=$\frac{10×2+2-10}{2}$=6,
F具有如下特点:①遇FeCl3有显色反应,说明含有酚羟基;②核磁共振氢谱中显示五种吸收峰说明含有5种类型的H原子;③苯环上的一氯代物只有两种,说明取代位置为对位;④除苯环外,不含有其他环状结构,则F分子中应含有1个C≡C或2个C=C,则可能的结构为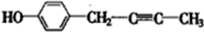 、
、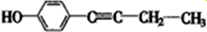 、
、 、
、 ,
,
(1)通过以上分析知,B的分子式为C12H12O2,
故答案为:C12H12O2;
(2)通过以上分析知,反应④的反应类型是酯的水解反应(或取代反应),E为CH3COOH,E的化学名称是乙酸,
故答案为:酯的水解反应(或取代反应);乙酸;
(3)反应③的化学方程式为 CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O,
故答案为:CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O;
(4)A为CH3COOCHBrCH3,A中的Br原子被H原子取代后的物质有多种同分异构体,其中能与NaHCO3溶液反应生成CO2的,说明有羧基,结构为CH3CH2CH2COOH、(CH3)2CHCOOH,共有2种,能发生银镜反应的,说明有醛基或甲酸某酯,其结构有HCOOCH2CH2CH3、HCOOCH(CH3)2,共2种,
故答案为:2;2;
(5)通过以上分析知,符合条件的F同分异构体有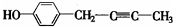 、
、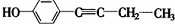 、
、 、
、 ,
,
故答案为: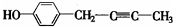 、
、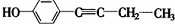 、
、 、
、 (任写两种).
(任写两种).
点评 本题考查有机物推断,侧重考查分析、推断能力,以C和新制氢氧化铜悬浊液发生氧化反应为突破口采用正逆结合的方法进行推断,注意灵活运用题给信息进行解答,难点是同分异构体种类的判断,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 水蒸气冷凝成水 | B. | 乙烯聚合成聚乙烯 | ||
| C. | 2NO2(g)?N2O4(g) | D. | CaCO3(s)?CaO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由Al、Cu、浓硝酸组成的原电池,其负极反应式为:Cu-2e-=Cu2+ | |
| B. | 由Al、Mg、NaOH组成的原电池,其负极反应式为:Al-3e-+3OH-=Al(OH)3↓ | |
| C. | 由Al、Mg、稀硫酸组成的原电池,其负极反应式为:Al-3e-=Al3+ | |
| D. | 由Fe、Cu、FeCl3组成的原电池,其正极反应式为:Cu-2e-=Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
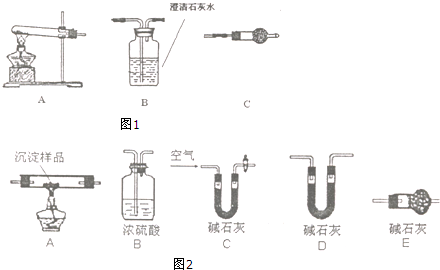
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
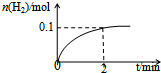 化学平衡:
化学平衡:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

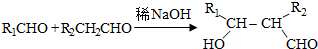
 .
. .
. ;
; (写结构简式)
(写结构简式)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
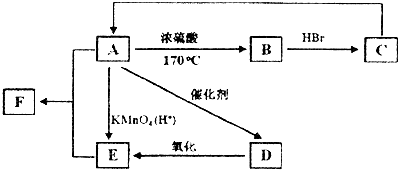
 ,
,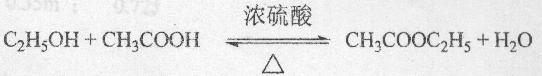 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3═K++Cl5-+3O2- | B. | HNO3═H++NO3- | ||
| C. | Na2CO3═Na2++CO32- | D. | CaCl2═Ca2++Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com