
【题目】下列叙述正确的是 ( )
A.恒容密闭容器中进行的反应3A(g) ![]() B(g)+c(g),在其他条件不变的情况下, 再充入一定量的A气体,A的转化率将增大
B(g)+c(g),在其他条件不变的情况下, 再充入一定量的A气体,A的转化率将增大
B.对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加
2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加
C.将A1C13溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为A1203
D.反应NH3(g)+HCl(g) ![]() NH4C1(s) ΔH<O在任何条件下均能自发进行
NH4C1(s) ΔH<O在任何条件下均能自发进行
科目:高中化学 来源: 题型:
【题目】下列有关品格能的说法错误的是( )
A.晶格能越大,离子晶体越稳定
B.晶格能越大,离子晶体的硬度越小
C.晶格能越大,离子晶体的能量越低
D.晶格能越大,离子晶体的熔点越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中,常用氯化铁溶液作为印刷电路铜板蚀刻液。请按要求回答下列问题:
(1)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:______________________________________,该过程中调节溶液的pH为5,则c(Fe3+)为:____________mol·L-1。(己知:Ksp[Fe(OH)3]= 4.0×10-38)
(2)某探究小组设计如下线路处理废液和资源回收:
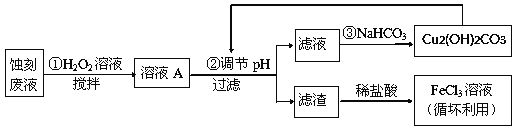
①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:_______________。
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:_________________。
③步骤①中加入H2O2溶液的目的是:______________________________________。
④已知:生成氢氧化物沉淀的pH
Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 4.7 | 7.0 | 1.9 |
沉淀完全时 | 6.7 | 9.0 | 3.2 |
根据表中数据推测调节pH的范围是:________________。
⑤写出步骤②中生成CO2的离子方程式:__________(已知Cu2(OH)2CO3难溶于水)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是( )
A.聚乙烯可发生加成反应
B.石油干馏可得到汽油、煤油等
C.丁烷的沸点低于丙醇
D.苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为了验证CH4是否具有还原性,设计了如下实验:
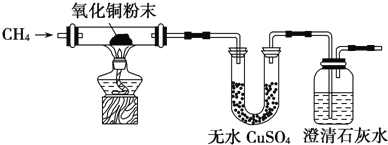
(1)实验过程中观察到无水CuSO4逐渐变蓝,澄清石灰水出现浑浊现象,则CH4与CuO反应的化学方程式为________________________________;
(2)研究小组将CH4通入溴水时,发现溴水逐渐褪色,你认为原因可能是___________________;请设计一个实验方案证明你的结论(用文字表示,不必画实验装置图)_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,回答下列问题:
(1)还原产物是
(2)氧化剂与还原剂的物质的量之比是
(3)用双线桥标上电子转移的方向和数目 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然碱(纯净物)可看作由CO2和NaOH反应后的产物所组成。称取天然碱样品四份溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO2的体积(标准状况)如下表:
Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
盐酸液的体积(mL) | 30 | 30 | 30 | 30 |
样品(g) | 2.26 | 3.39 | 5.65 | 6.78 |
二氧化碳的体积(mL) | 448 | 672 | 784 | 672 |
(1)由以上数据,可以推测用1.13g样品进行同样的实验时,产生CO2______mL(标准状况).
(2)另取2.26g天然碱样品于300℃加热分解至完全(300℃时NaCO3不分解),产生CO2 112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式_________.
(3)依据上表所列数据以及天然碱的化学式,试求盐酸的浓度_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动。当燃料气为C2H4时,其正极、负极反应式分别为

正极:______________________;
负极:____________________。
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为__________________;除去甲醇的离子方程式为___________。
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为______________________;
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为___________L(标准状况)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com