
| A. | 它的原子半径比钠大,失电子能力不如钠 | |
| B. | 它的金属性比钠强,跟水反应会更剧烈 | |
| C. | 它的氢氧化物(FrOH)是一种强碱,遇酚酞溶液变红 | |
| D. | 它可与硫酸铜溶液反应,但是不易得到金属铜 |
分析 根据碱金属的性质递变进行分析判断,同主族从上到下原子半径依次增大,金属性增强,氢氧化物碱性依次增强,与水反应的剧烈程度依次增大,据此分析.
解答 解:A、同主族从上到下原子半径依次增大,金属性增强,则它的原子半径比钠大,失电子能力也比钠强,故A错误;
B、同主族从上到下金属性增强,失电子能力比钠强,则跟水反应会更剧烈,故B正确;
C、Fr处于第ⅠA族,最外层电子数为1,最高正化合价为+1,它的氢氧化物化学式为FrOH,同主族从上到下金属性增强,碱性比KOH强,遇酚酞溶液变红,故C正确;
D、同主族从上到下金属性增强,失电子能力比钠强,则跟水反应会更剧烈,所以与硫酸铜溶液反应,先与水反应,不易得到金属铜,故D正确;
故选A.
点评 本题考查同主族元素的性质的递变规律,注意同主族元素既具有性质的相似性,又具有递变性,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 58 | B. | 173 | C. | 3 | D. | 128 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KI被氧化成KOH | |
| B. | KI是离子化合物,I2是共价化合物 | |
| C. | 1 mol O3 在反应中得到4 mol 电子 | |
| D. | KOH中既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
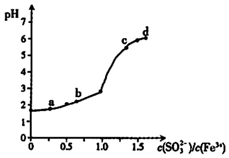 向FeCl3溶液中加入Na2SO3溶液,测定混合后溶液pH随混合前溶液中$\frac{c(S{O}_{3}^{2-})}{c(F{e}^{3+})}$变化的曲线如图所示.实验发现:
向FeCl3溶液中加入Na2SO3溶液,测定混合后溶液pH随混合前溶液中$\frac{c(S{O}_{3}^{2-})}{c(F{e}^{3+})}$变化的曲线如图所示.实验发现:| A. | 向a点溶液中滴加BaCl2溶液,无明显现象 | |
| B. | b点较a点溶液pH升高的主要原因:2Fe3++SO32-+H2O═2Fe2++SO42-+2H+ | |
| C. | c点溶液中发生的主要反应:2Fe3++3SO32-+6H2O?2Fe( OH)3+3H2SO3 | |
| D. | 向d点上层清液中滴加KSCN溶液,溶液变红;再滴加NaOH溶液,红色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯、氯乙烯、苯乙炔分子内所有原子一定在同一平面上 | |
| B. | 苯、乙烯、聚乙烯都能发生加成反应,也能发生氧化反应 | |
| C. | 等质量的乙烯和乙醇完全燃烧,消耗氧气的物质的量相等 | |
| D. | 分子式为C5H10O2,能发生水解反应但不能发生银镜反应的有机物有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与K+、Na+、AlO2-、CO32-可以大量共存 | |
| B. | 可用铁氰化钾溶液检验该溶液是否变质 | |
| C. | 与100mL 0.1mol/L Ba(OH)2反应的离子方程式:Ba2++2OH-+SO42-+2NH4+═BaSO4↓+2NH3•H2O | |
| D. | 与足量酸性KMnO4溶液混合充分反应,共转移电子0.01mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com