
以惰性电极电解一定浓度的CuSO4溶液,一段时间后取出电极,加入9.8 g Cu(OH)2后溶液与电解前相同,则电解时电路中流过的电子为
A.0.1mol B.0.2mol C.0.3mol D.0.4mol
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
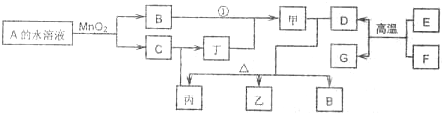
科目:高中化学 来源:同步题 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:
(09盐城第三次调研)一些较活泼的金属在某些特定的介质环境中,会变为惰性状态,这是由于金属表面上覆盖了一层氧化膜。铁在不同浓度的硝酸中溶解与钝化情况如图如示。试探究下列问题:
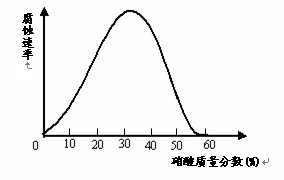
(1)现有一枚光亮的铁钉,欲使其表面形成钝化层,应将其放入浓度大于 的硝酸中一段时间;证明其表面已形成一层致密的钝化层的简单实验是: 。
(2)下列有关说法不正确的是 (选填序号)。
![]()
A.铜难溶于冷的浓硫酸,是因为铜在浓硫酸中发生钝化
B.铜片和铝片用导线连接后插入冷的浓硝酸中,电流一定总是由铜电极沿导线流入铝极
C.铁在硝酸溶液中的腐蚀速率与硝酸浓度一定呈正比
D.可用冷的浓硝酸除去铝制容器内的水垢
(3)发蓝液是由NaNO3、NaNO2及NaOH配成的,在加热条件下,通过三步反应使铁表面生成一层致密的Fe3O4:3Fe+NaNO2+5NaOH![]() 3Na2FeO2+H2O+NH3↑…………①;
3Na2FeO2+H2O+NH3↑…………①;
8Fe+3NaNO3+5NaOH+2H2O![]() 4Na2Fe2O4+3NH3↑……②;
4Na2Fe2O4+3NH3↑……②;
以及第三步生成四氧化三铁。请补充第三步反应的方程式并配平: 。
(4)为了使铝表面形成较厚的氧化膜,工业上常用电解硫酸溶液的方法,在阳极上生成氧化铝,写出此时阳极的电极反应: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com