
【题目】CuSO4是一种重要的化工原料, 其有关制备途径及性质如图所示,其中混合气体 X中含有SO2、SO3。下列说法不正确的是
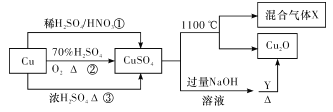
A. 途径①所用混酸中 H2SO4与 HNO3物质的量之比最好为 3∶2
B. 相对于途径①、 ③,途径②更好地体现了绿色化学思想
C. 1 mol CuSO4在 1100℃所得混合气体X中O2为 0.75 mol
D. Y 可以是葡萄糖
【答案】C
【解析】途径①涉及反应为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;途径②涉及反应为2Cu+2H2SO4+O2=2CuSO4+2H2O;途径③涉及反应为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,根据反应的离子方程式或化学方程式评价制备方案。
CuSO4+SO2↑+2H2O,根据反应的离子方程式或化学方程式评价制备方案。
A.Cu与混酸反应,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,离子反应为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,从方程式知,硝酸根离子由硝酸提供,氢离子由硝酸和硫酸提供,所以硝酸为2mol时,硫酸为3mol,用混酸中H2SO4与HNO3物质的量之比最好为3:2,选项A正确;
B.相对于途径①、③,途径②的优点:制取等质量胆矾需要的硫酸少、途径②无污染性气体产生,选项B正确;
C.根据2CuSO4![]() Cu2O+SO2↑+SO3↑+O2↑知,1molCuSO4在1100℃所得混合气体X中O2为0.5mol,二氧化硫0.5mol,三氧化硫0.5mol,共1.5mol,选项C不正确;
Cu2O+SO2↑+SO3↑+O2↑知,1molCuSO4在1100℃所得混合气体X中O2为0.5mol,二氧化硫0.5mol,三氧化硫0.5mol,共1.5mol,选项C不正确;
D.葡萄糖与氢氧化铜反应的方程式为:C6H12O6+2Cu(OH)2=C6H12O7+Cu2O+2H2O,所以Y可为葡萄糖,也可以是含醛基的有机物,选项D正确。答案选C。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与完成相关实验问题讨论. 【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯.
【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置:
根据分析回答:
(1)三位同学设计的装置中最不合理的是(选填“甲”或“乙”或“丙”),原因是 .
(2)【实验步骤】 a.按所选择的装置组装仪器,在试管①中先加入3mL乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸;
b.将试管固定在铁架台上;
c.在试管②中加入适量的饱和Na2CO3溶液;
d.用酒精灯对试管①加热;
e.当观察到试管②中有明显现象时停止实验.
试管①中加入浓硫酸的作用是
(3)该实验中长导管的作用是 .
(4)试管②中饱和Na2CO3溶液的作用是;可否用NaOH溶液代替Na2CO3溶液?(填“是”或“否”),理由是 .
(5)试管②中观察到的现象是;从试管②中分离出乙酸乙酯的实验操作名称是 .
(6)分别写出试管①和②中发生反应的化学方程式 ①;
② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯原子的结构示意图为_____________________。
(2)![]() 微粒中的质子数是_______,中子数是_______,核外电子数是_______。
微粒中的质子数是_______,中子数是_______,核外电子数是_______。
(3)49g 硫酸的物质的量为________mol,其完全电离产生H+的个数为___________。
(4)V L Al2(SO4)3溶液中,含有a g Al3+,则溶液中Al3+的物质的量浓度_________;SO42 物质的量浓度__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体.
(1)4CO(g)+2NO2(g)═4CO2(g)+N2(g)△H=﹣1 200kJmol﹣1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是(填代号).
(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:
CO(g)+H2O(g)CO2(g)+H2(g)△H<0.
820℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0.
起始物质的量 | 甲 | 乙 | 丙 |
n(H2O)/mol | 0.10 | 0.20 | 0.20 |
n(CO)/mol | 0.10 | 0.10 | 0.20 |
①该反应的平衡常数表达式为 .
②平衡时,甲容器中CO的转化率是 . 比较下列容器中CO的转化率:乙甲;丙甲(填“>”、“=”或“<”).
③丙容器中,通过改变温度,使CO的平衡转化率增大,则温度(填“升高”或“降低”),平衡常数K(填“增大”、“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法不利于金属防护的是( )
A. 菜刀切菜后不洗净就放回刀架
B. 将钢铁制成不锈钢
C. 在铁塔的表面喷上一层油漆
D. 埋在地下的钢管与锌块连接
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
实验编号 | HA物质的量浓度 | NaOH物质的量浓度 | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸 .
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2(选填“是”或“否”).混合液中离子浓度c(A﹣)与 c(Na+)的大小关系是 .
(3)丙组实验结果分析,HA是酸(选填“强”或“弱”).该混合溶液中离子浓度由大到小的顺序是 .
(4)丁组实验所得混合溶液中由水电离出的c(OH﹣)=molL﹣1 . 写出该混合溶液中下列算式的精确结果(不需做近似计算).c(Na+)﹣c(A﹣)=molL﹣1 c(OH﹣)﹣c(HA)=molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标准盐酸溶液滴定未知浓度的NaOH溶液,下列各操作中,会引起实验误差的是( )
A.取干燥洁净的酸式滴定管立即装入标准盐酸
B.用蒸馏水洗净锥形瓶后,立即装入一定体积的NaOH溶液后进行滴定
C.往盛有20.00mL NaOH溶液的锥形瓶中,滴入几滴酚酞指示剂后进行滴定
D.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,然后装入一定体积的NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com