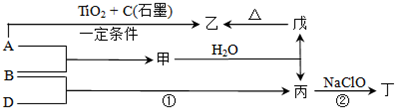
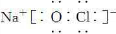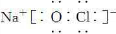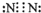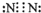解:戊的原子最外层电子数比次外层少2个,应为S元素,丙与戊,则丙为O元素,甲与乙可以按照原子个数比3:1形成化合物A,且每个A分子中含有10个电子,应为NH
3,则甲为H元素,乙为N元素,甲与丁,根据原子序数关系可知丁为Na元素,
(1)由以上分子可知戊为S,原子核外有3个电子层,最外层电子数为3,则原子结构示意图为

,乙单质为N
2,电子式为
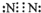
,
故答案为:

;
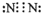
;
(2)氨气水溶液中存在NH
3?H
2O,为弱电解质,可电离出OH
-,溶液呈碱性,离子方程式为NH
3?H
2O?NH
4++OH
-,
故答案为:NH
3?H
2O?NH
4++OH
-;
(3)甲与丁可形成一种离子化合物为NaH,与水反应的方程式为NaH+H
2O=NaOH+H
2↑,该反应中,氧化剂是H
2O与还原剂是NaH,由方程式可知二者物质的量之比是1:1,故答案为:1:1;
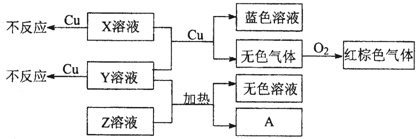
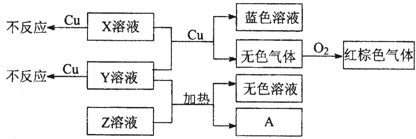
(4)Y溶液与Z溶液加热生成NH
3,则Y溶液与Z溶液为铵盐与碱.X溶液、Y溶液单独与铜不反应,二者混合能与铜反应生成无色气体,该气体与氧气反应呈红棕色,所以红棕色气体为NO
2,无色气体为NO,所以X溶液、Y溶液为硝酸盐与酸,由于Y溶液与Z溶液为铵盐与碱,所以Y为硝酸铵,Z为氢氧化钠,X为硫酸.
①Y为硝酸铵溶液,Z为NaOH溶液,二者在加热条件下可反应氨气,
反应的离子方程式为NH
4++OH
-
NH
3↑+H
2O,
故答案为:NH
4++OH
-
NH
3↑+H
2O;
②Cu与X、Y的混合溶液反应的离子方程式是3Cu+8H
++2NO
3-=3Cu
2++2NO↑+4H
2O,
故答案为:3Cu+8H
++2NO
3-=3Cu
2++2NO↑+4H
2O.
分析:戊的原子最外层电子数比次外层少2个,应为S元素,丙与戊,则丙为O元素,甲与乙可以按照原子个数比3:1形成化合物A,且每个A分子中含有10个电子,应为NH
3,则甲为H元素,乙为N元素,甲与丁,根据原子序数关系可知丁为Na元素,结合对应元素化合物的性质以及题目要求可解答该题.
点评:本题考查无机物的推断,侧重于元素周期表位置与原子结构关系的考查,题目难度中等,注意正确推断元素的种类为解答本题的关键.

 ,乙单质为N2,电子式为
,乙单质为N2,电子式为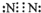 ,
, ;
;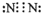 ;
; NH3↑+H2O,
NH3↑+H2O, NH3↑+H2O;
NH3↑+H2O;