
���� ��1���ڳ�ʪ�Ļ����У������γ�ԭ��ض������绯ѧ��ʴ����ֹ��ʴ�ķ����У�����������ˮ���ı����ʽṹ�ȣ�
��2��������ϳɲ��ϡ�ָ�������ϡ��ϳ���ά���ϳ������������Ƿ��ۻ�����Ϊ���������Ϻ��ȹ������ϣ�
��3�������Ĵ��������Ƿ��ա����ѷʣ�
��� �⣺��1���ڳ�ʪ�Ļ����У�����̼�͵������Һ����ԭ��ض�����������������Ҫ�����绯ѧ��ʴ�����õķ����У���ơ�Ϳ��֬��Ϳ��ȣ�������ˮ�Ļ�ѧ�����У��кͷ�����ѧ��������������ԭ����
�ʴ�Ϊ���绯ѧ����ơ�Ϳ��֬���кͷ�����ѧ��������������ԭ����
��2������ϳɲ�����ָ���ϡ��ϳ��ͺϳ���ά�����������������Ϻ��ȹ������������࣬��ȩ��֬�����ȹ������ϣ�����ϩ�����������������ϣ�
�ʴ�Ϊ�����ϣ��ϳ����ϳ���ά�������ԣ��ȹ��ԣ��ȹ��ԣ������ԣ�
��3����������ͨ�����õ����ִ��������ǣ����ա����ѷʣ��ʴ�Ϊ�����գ����ѷʣ�
���� ���⿼�黷����Ⱦ�������������ڻ�ѧ�����彡���Ŀ��飬Ϊ�߿��������ͺ�Ƶ���㣬����������ѧ�������ÿ�ѧ�������ѶȲ���ע����ػ���֪ʶ�Ļ��ۣ�


 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д� Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͬ��ͬѹʱ����ͬ������κ����嵥��������ԭ����Ŀ��ͬ | |
| B�� | ��״���£�22.4 Lˮ������ˮ������ΪNA | |
| C�� | �ڳ��³�ѹ�£�11.2 L����������ԭ����ĿΪNA | |
| D�� | 34g��������������ĿΪ20 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 28 g���������е�ԭ����ĿΪ2 NA | |
| B�� | 4 g�����Ʊ�ɸ�����ʱʧȥ�ĵ�����ĿΪ0.1 NA | |
| C�� | 1 mol�����������NA��������ӵ�����֮����� | |
| D�� | ��״���£�22.4 L�������ϩ����������ķ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡ��Һ��1mol���1mol����ȫ��Ӧ���ų��������������к��� | |
| B�� | ��101kPʱ1mol����ȼ��ʱ���ų����������������ʵ�ȼ���� | |
| C�� | �Ȼ�ѧ����ʽ�У�������ǰ�Ļ�ѧ����������ʾ���Ӹ��� | |
| D�� | ����ͬ�����£�1 molH20��l����ȫ�ֽ����յ�������H2��O2��������1 molH2O��g���ų���������ֵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��صĵ��ҺΪ������Һ������ΪNi2O3������ΪFe | |
| B�� | ��طŵ�ʱ��������ӦΪFe+2OH--2e-=Fe��OH��2 | |
| C�� | ��س��ʱ��������ӦΪ2Ni��OH��2+2OH--2e-=Ni2O3+3H2O | |
| D�� | ��س������У�����������Һ��pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
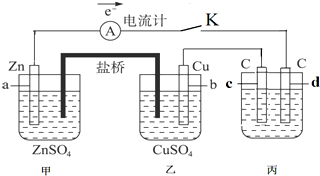
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ����ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ�в�����ȷ���ǣ�������
����ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ�в�����ȷ���ǣ�������| X | Y | Z | |
| A | ǿ����� | ����� | ������ |
| B | ���� | ��ɢϵ | ����� |
| C | �û���Ӧ | ������ԭ��Ӧ | ���ӷ�Ӧ |
| D | ���������� | ���������� | ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com