
| A. | 80mL10mol/L的浓盐酸与足量的MnO2加热反应,产生Cl2分子数约为0.2NA | |
| B. | 一定条件下,将1molN2和3molH2混合,充分反应后转移电子数为6NA | |
| C. | 钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1NA | |
| D. | 常温常压下,等质量的CO和N2中含有原子数目均为2NA |
分析 A.二氧化锰只能与浓盐酸反应,与稀盐酸不反应;
B.氮气与氢气合成氨气为可逆反应,可逆反应不能进行到底;
C.钠发生氧化反应后,Na元素的化合价由0升高为+1价;
D.CO和N2相对分子质量都是28,都是双原子分子;
解答 解:A.二氧化锰只能与浓盐酸反应,与稀盐酸不反应,故80mL10mol/L的浓盐酸不能反应完全,即生成的氯气的分子数小于0.2NA,故A错误;
B.一定条件下,将1molN2和3molH2混合,充分反应后生成的氨气小于2mol,转移电子数小于6NA,故B错误;
C..23g钠充分燃烧时转移电子数为$\frac{23g}{23g/mol}$×(1-0)×NA=1NA,故C正确;
D.CO和N2相对分子质量都是28,都是双原子分子,所以等质量的CO和N2中含有原子数目均为2NA,故D正确;
故选:CD.
点评 本题考查阿伏伽德罗常数及计算,为高频考点,把握以物质的量为核心的计算公式是解题关键,注意可逆反应特点,注意二氧化锰与盐酸反应条件,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
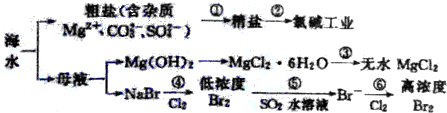
| A. | 过程①的提纯只有物理过程,过程②通过氧化还原反应可产生两种单质 | |
| B. | 在过程③中将MgCl2•6H2O直接灼烧即可制得纯净无水MgCl2 | |
| C. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 | |
| D. | 过程⑥所得的高浓度溴水只需分液即可获得液溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与氟气发生取代反应可以制得CH3F | |
| B. | CH3F分子中含有离子键 | |
| C. | CH3F分子中含有共价键和离子键 | |
| D. | CH3F的摩尔质量是34 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 科学家研制的离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高、更安全、环保.下列说法不正确的是( )
科学家研制的离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高、更安全、环保.下列说法不正确的是( )| A. | 羟基硝酸铵中阳离子的各原子共平面 | |
| B. | 羟基硝酸铵易溶于水 | |
| C. | 羟基硝酸铵中含有离子键和共价键 | |
| D. | 9.6g羟基硝酸铵中含有0.2mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
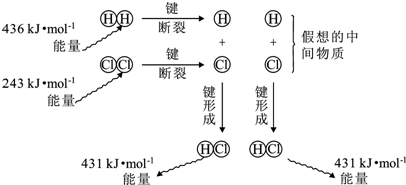
| A. | H-H键比Cl-Cl键强,H-Cl键是极性共价键 | |
| B. | 断键吸收能量,成键释放能量,该反应△H=-183kJ/mol | |
| C. | 若生成液态HCl,则反应释放的能量将减少 | |
| D. | 反应的焓变与假想的中间物质的种类、状态无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com