
【题目】某兴趣小组查阅资料得知工业上常采用蒽醌法生产 H2O2,其原理与流程如图所示:
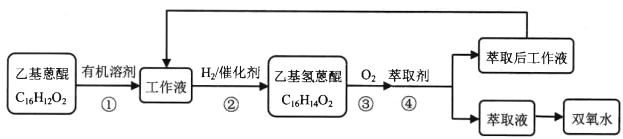
下列说法不正确的是
A. 蒽醌法制备 H2O2理论上消耗的原料是H2、O2,乙基蒽醌可循环使用
B. 步骤②为还原反应,步骤③为氧化反应
C. 步骤④中可选用 CCl4作为萃取剂
D. 应除净萃取后工作液残留的H2O2,否则释放的氧气与氢气混合易爆炸
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习。下列关于物质的类别中,不正确的是(括号内为类别)( )
A.H2O(氧化物)B.H2SO4(含氧酸)
C.CH3COOH(混合物)D.I2的CCl4溶液(混合物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如右下图(二茂铁熔点是173℃,在100℃时开始开华;沸点是249℃)。实验步骤为:
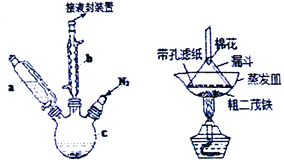
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(密度0.95g/cm3),搅拌;
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入仪器d,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是______________,作用是________________________。
(2)步骤①中通入氮气的目的是__________________________________。
(3)仪器c的适宜容积应为_________:①100mL、②250mL、③500mL;仪器a使用前应进行的操作是_______________________________________。
(4)KOH、FeCl2、C5H6反应生成二茂铁[Fe(C5H5)2]和KCl的化学方程式为_________________________;步骤⑦是二茂铁粗产品的提纯,该过程在右图中进行,其操作名称为 ____________________________。
(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是_________________________。
(6)最终得到纯净的二茂铁3.7g,则该实验的产率为 __________________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固态或气态碘分别与氢气反应的热化学方程式如下:
① H2(g) +I2(?)![]() 2HI(g) △Hl=-9.48kJ/mol
2HI(g) △Hl=-9.48kJ/mol
②H2(g) +I2(?)![]() 2HI(g) △H2=+26.48kJ/mol
2HI(g) △H2=+26.48kJ/mol
下列判断不正确的是
A. ①中的I2为气态,②中的I2为固态
B. ②的反应物总能量比①的反应物总能量低
C. 反应①的产物比反应②的产物热稳定性更好
D. lmol固态碘升华时将吸热35.96kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按以下步骤从![]() 。(部分试剂和反应条件已略去)
。(部分试剂和反应条件已略去)

请回答下列问题:
(1)A的名称为________________。
(2)分别写出 B、D 的结构简式:B_________________、D__________________。
(3)反应①~⑦中属于消去反应的是__________。
(4)D与Br2按1:2反应的产物的结构简式为________________。
(5)试写出 C―→D 反应的化学方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,草酸铜晶体(CuC2O4· xH2O)受热分解的化学方程式为: CuC2O4· xH2O·![]() CuO+CO↑ +CO2↑ +xH2O↑。某化学兴趣小组设计如图装置,探究草酸铜晶体分解的气体产物:
CuO+CO↑ +CO2↑ +xH2O↑。某化学兴趣小组设计如图装置,探究草酸铜晶体分解的气体产物:
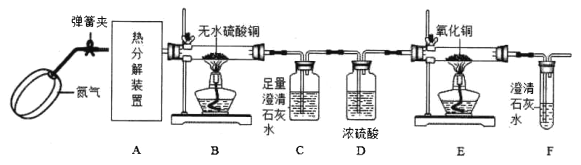
请回答:
(1)该套实验装置的明显缺陷是________。
(2)实验过程中观察到B中白色无水硫酸铜变成蓝色,C、F中澄清石灰水变浑浊,E中________ (填实验现象),则可证明草酸铜晶体热分解的气体产物是H2O、CO、CO2。
(3)该兴趣小组改变热分解反应条件,完全反应后发现C中白色沉淀量明显较先前实验多,而E、F中未见明显现象,请推测A装置中固体产物成分并设计一个实验方案,用化学方法验证固体产物________ (不考虑操作和药品的问题)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10﹣9m,其研究成果广泛应用于催化及军事科学中,“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是( )
A.有丁达尔效应
B.能全部透过半透膜
C.不能透过滤纸
D.所得分散系不稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将燃煤废气中的CO2转化为二甲醚的反应为:2CO2(g)+6H2(g)![]() CH3OCH3(g+3H2(g) △H
CH3OCH3(g+3H2(g) △H
已知:①CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.7kJ.mol-l
CH3OH(g) △H1=-90.7kJ.mol-l
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-23.5kJ.mol-l
CH3OCH3(g)+H2O(g) △H2=-23.5kJ.mol-l
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2=-41.2kJ.mol-l
CO2(g)+H2(g) △H2=-41.2kJ.mol-l
(1)△H_____ kJ.mol-l
(2)某温度下,在体积固定为2L的密闭容器中进行反应①,将1molCO和2molH2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P前/P后) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则达到平衡时CO的转化率为_________。
(3)已知在某压强下,该反应在不同温度、不同投料比[n(H2)/n(CO2)]时,CO2的转化率如右图所示。从图中可得出三条主要规律:
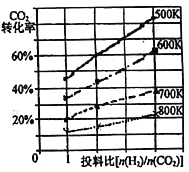
①增大投料比,CO2的转化率增大;②_____________;③_______________。
(4)反应③的v-t图像如图1所示,若其他条件不变,只是在反应前增大容器体积使压强减小,则其v-t图像如图2所示。
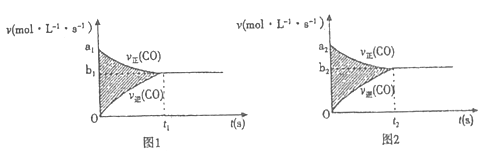
下列说法正确的是________。
①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦ t1<t2 ⑧两图中阴影部分面积相等⑨右图阴影部分面积更大 ⑩左图阴影部分面积更大
A. ①③⑦⑧ B. ①③⑤⑧ C. ②④⑦⑨ D. ①③⑦⑩
(5)由甲醇液相脱水法也可制二甲醚,首先将甲醇与浓硫酸反应生成硫酸氢甲酯(CH3OSO3H):CH3OH+H2SO4→CH3OSO3H+H2O;生成的硫酸氢甲酯再和甲醇反应生成二甲醚,第二步的反应方程式为:____________。与CO2和H2反应制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com