
【题目】向NaHCO3溶液中加入Na2O2,发生反应的离子方程式依次为:________________________________, _____________________________。
科目:高中化学 来源: 题型:
【题目】下列有关氨和铵盐的叙述正确的是
A. NH3易液化,常用作制冷剂
B. NH4Cl中含有少量的I2可通过加热的方法除去
C. 将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
D. 某气体通入紫色石蕊试液后.溶液变红,据此可推断该气体为NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁元素和碳元素形成的单质及化合物在生产、生活中有广泛的用途,
请回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为_________________;其最外层电子的电子云形状为___________。
(2)(NH4)2Fe(SO4)2 6H2O俗称摩尔盐。其阴离子的VSEPR模型名称为____________________。
写出一种与NH4+互为等电子体的分子的电子式:________________________________。
(3)Fe(CO)5可用作催化剂、汽油抗暴剂等.其分子中σ键和π键的数目之比为______________。CO的沸点高于N2的原因是_________________________。
(4)碳元素可形成多种单质。
①石墨烯是从石墨中剥离出来的由单层碳原子构成的平面结构新型碳材料。其中碳原子的杂化方式为______________________。
料,其中碳原子的杂化方式为 ,
②金刚石的晶胞如图所示。若晶胞参数为a pm,阿伏加德罗常数的值为NA,则该晶胞中原子的体积占晶胞体积的百分率为________________;1cm3晶体的平均质量为___________(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiCl4是制备钛及其化合物的重要中间体,某小组同学利用下列装置在实验室制备TiCl4,设计实验如下(夹持装置略去);
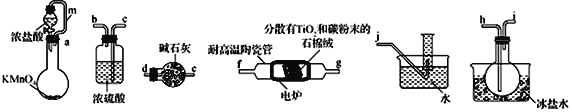
相关信息如下表所示:
熔点/℃ | 沸点/℃ | 密度/(g cm-3) | 水溶性 | |
TiCl4 | -25 | 136 | 1.5 | 易水解,能溶于有机溶剂 |
CC14 | -23 | 76.8 | 1.6 | 难溶于水 |
请回答下列问题:
(1)按照气流由左到右的方向,上述装置合理的连接顺序为_____________(填仪器接口字母)
(2)根据完整的实验装置进行实验,实验步骤如下:检査装置气密性后,装入药品;_____________
(按正确的顺序填入下列操作的字母)。
A.关闭分液漏斗活塞 B.停止加热,充分冷却
C.打开分液漏斗活塞 D.加热装置D中陶瓷管
实验时,当观察到______________时,开始进行步骤D。
(3)装置A中导管m的作用为_______________________。
(4)装置C的作用为 ___________________________________________。
(5)装置D中除生成TiCl4外,同时生成一种气态不成盐氧化物,该反应的化学方程式为__________________________________。
(6)设计实验证明装置 F中收集到的液体中含有TiCl4:______________________________________________。
(7)制得的TiCl4中常含有少量CCl4,从混合液体中分离出TiCl4的操作名称为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的晶体有如下类型:①分子晶体;②离子晶体;③原子晶体;④金属晶体。短周期非金属元素所形成的单质或化合物中,固态时的晶体类型可能是
A.①③B.①③④C.①②③D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按下图进行实验,在A中放的是干燥的红色纸条,B中放的是湿润的红色纸条,C中盛放的是氢氧化钠溶液。请回答下列问题。
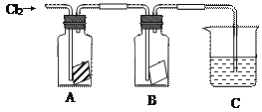
(1)通入Cl2一段时间后,A、B装置中,红色纸条的现象和结论为:
装置 | 现象 | 结论 |
A | ______________ | 潮湿的氯气______(填能或不能)使红色纸条褪色,因为反应生成的____________具有漂白性 |
B | ______________ |
(2)C装置的作用是__________________________
写出装置C中反应的化学方程式:_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA是阿伏加德罗常数的值,下列说法正确的是
A. 4.6g NO2(g)和N2O4(g)的混合物中含有0.3NA个原子
B. 0.1mol乙酸与足量乙醇发生酯化反应,生成0.1NA个乙酸乙酯分子
C. 常温下将5.6gFe投入足量浓硫酸,电子转移数为0.3NA
D. Na2O2与足量H2O发生反应,每生成2.24L气体(标准状况),电子转移数0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。吸入CO2时,其工作原理如下图所示。吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法不正确的是( )

A. 放电时电池总反应是4Na+3CO2 = 2Na2CO3+C
B. “吸入”CO2时的正极反应:4Na++3CO2+4e-=2Na2CO3+C
C. “呼出”CO2时钠箔电极反应式是Na++e-=Na
D. 每“呼出”22.4LCO2,转移电子数为4/3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2 和AlCl3的混合溶液aL,将它平均分成两份。一份滴加稀硫酸,使钡离子完全沉淀,另一份滴加AgNO3溶液,使氯离子完全沉淀。反应中消耗x mol H2SO4,y mol AgNO3溶液。据此得知原混合溶液中的铝离子浓度为( ) mol/L。
A. (y-2x)/a B. (y-x)/a C. 2(y-2x)/3a D. (y-2x)/3a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com