
��16�֣�̼���仯����Ӧ�ù㷺��
I ��ҵ������CO��ˮ������Ӧ����������������ƽ�⣺
CO(g)+H2O(g)  CO2(g)+H2(g) ��H��0
CO2(g)+H2(g) ��H��0
��1����1L�����ܱ�������ע��CO(g)��H2O(g),830��ʱ��ò����������±�������¶��·�Ӧ��ƽ�ⳣ��K=______________��
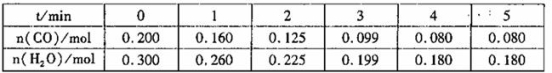
��2����ͬ�����£���1L�����ܱ������У�ͬʱע��2mol CO��2mol H2O(g),1molCO2��1mo1H2����ʱv(�� ) __________v(��)(���������������)
��3��������Ӧ�ﵽƽ��ʱ��Ҫ���CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��_______������ĸ���ţ���
A�������¶�
B���������
C������ѹǿ
D������CO��Ũ��
E����ʱ�����CO2
II ��֪CO(g)+1/2 O2 (g)��CO2 (g) ��H��һ141 kJ��mol-1
2H2(g)+ O2(g)��2H2O(g) ��H��һ484 kJ��mol-1
CH3OH��1��+3/2O2 (g)��CO2(g)+2H2O(g) ��H��һ726 kJ��mol-1
��4����CO(g)��H2(g)�����Ƶ�Һ̬�״����Ȼ�ѧ����ʽΪ___________________________��
IIIijͬѧ�����һ���״�ȼ�ϵ�أ����øõ�ص��100mLһ��Ũ��NaCl��CuSO4�����Һ����װ����ͼ��

��5��д������ͨ��״���һ���ĵ缫��Ӧʽ__________________________________ ��
��6������������������������������ʱ��仯�Ĺ�ϵ���ͼ��ʾ����������ѻ���ɱ�״���µ��������д����t1��,ʯī�缫�ϵĵ缫��Ӧʽ____________��ԭ�����Һ��CuSO4�����ʵ���Ũ��____________mol/L����������Һ������䣩
��7������t2ʱ���õ���Һϡ����200mL������Һ��pHԼΪ___________��
��1�� 1 ��2�֣� ��2������2�֣� ��3��A E ��2�֣�
��4��CO(g) + 2H2(g) == CH3OH��1�� ��H��101 kJ��mol-1 ��2�֣�
(5) CH3OH -- 6e- + 8OH- == CO32-+ 6H2O ��2�֣�
(6) 4OH-��4e-=2H2O+O2�� �� 2H2O��4e-=4H++O2����2�֣� 0.2��2�֣�
��7��1 ��2�֣�
��������
�����������1��CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼ���ʵ��� 0.200 0.300 0 0
�ı����ʵ��� 0.12 0.12 0.12 0.12
ƽ��ʱ���ʵ��� 0.08 0.18 0.12 0.12
ƽ�ⳣ��=0.12��0.12/0.08��0.18=1.��2��Qc=1��1/2��2=0.25<1�����Է�Ӧ��������У���������Ӧ���ʴ����淴Ӧ���ʡ���3�����һ����̼��ת���ʣ�Ҫ��ƽ�������ƶ������Կ������£���ʱ�����������̼��ѡAE������������ı����ʵ�ת���ʣ�����ѹǿ��ƽ�ⲻ�ƶ�����Ӱ��ת���ʣ�����һ����̼��Ũ�ȣ�ת���ʽ��͡���4������Ӧ���Ϊ�٢ڢۣ����ݸ�˹���ɣ���+��-�ۣ����Ȼ�ѧ����ʽΪ��CO(g) + 2H2(g) == CH3OH��1�� ��H��101 kJ��mol-1 ����5������ͨ��״���һ����Ϊԭ��صĸ������ڼ��������£�CH3OH -- 6e- + 8OH- == CO32-+ 6H2O ����6����Ϊ���أ�ʯī�缫����ԭ��ص�������Ϊ���ص��������տ�ʼ�������������������������Ϊ�������տ�ʼͭ���ӷŵ磬���Ը��ݱ�ͼ����Ϊ�������������壬��Ϊ�������������壬t1��ʯī�缫���Dz��������ĵ缫��Ӧ��4OH-��4e-=2H2O+O2�� �� 2H2O��4e-=4H++O2������ͼ��֪�õ�224������������ת�Ƶ���0.02Ħ����������336-224=112����������ת�Ƶ���0.005��4=0.02Ħ�������Ը��ݵ����غ㣬ͭ���ӵ����ʵ���=��0.02+0.02��/2=0.02Ħ��������ͭ����Ũ��=0.02/0.1=0.2 mol/L����7������2H2O��4e-=4H++O2��������112����������������0.02Ħ���������ӣ���������Ũ��=0.02/0.1=0.1mol/L,����pH=1.
���㣺��ѧƽ�ⳣ����Ũ�Ȼ��ͷ�Ӧ���еķ���ѧƽ���ƶ���ԭ��غ͵���ԭ����Ӧ�á�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ��һ12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪Na�Ļ��ϼ�ֻ��+1�ۣ�����NaH+H2O===NaOH+H2������˵����ȷ����
A��H2���ǻ�ԭ���� B��H2������������
C��NaH�е���Ԫ�ر���ԭ D�����������뻹ԭ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ�߶�12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��4 mol A�����2mol B������2L�������л�ϲ���һ�������·�����Ӧ��2A��g��+B��g�� 2 C��g������2s����C��Ũ��Ϊ0��6 mol��L��1�����м���˵������ȷ����
2 C��g������2s����C��Ũ��Ϊ0��6 mol��L��1�����м���˵������ȷ����
A��������A��ʾ��Ӧ��ƽ������Ϊ0��3 mol��L��1��s��1
B��������B��ʾ��Ӧ��ƽ������Ϊ0��3 mol��L��1��s��1
C��2 sʱ����A��ת����Ϊ70%
D��2 sʱ����B��Ũ��Ϊ0��3 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У��һ��ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ��Ӧ�����ӷ���ʽ�������
A����������ˮ��Cl2 + H2O 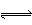 H+ + Cl�C + HClO
H+ + Cl�C + HClO
B����С�մ�����θ����ࣺHCO3-��H��===CO2����H2O��θ�����Ҫ�ɷ���ϡ���ᣩ
C����������ϡH2SO4��Ӧ��Fe + 2H+ == Fe3+ + H2��
D�������������������Һ��Ӧ��2Al��2OH����2H2O===2AlO2����3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У��һ��ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����к���Ԫ�أ��Ӻ�������ȡ�������²��裺��ͨ������Cl2���ڽ��������ճɻҺ��ˮ�� �裻�ۼ�CCl4�����÷�Һ©����Һ���ݹ��ˡ�������IJ���˳����
A���٢ڢۢܢ� B���ڢݢ٢ۢ�
C���٢ۢݢڢ� D���ڢ٢ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У�߶���ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
Ϊ��ǿ������ʴ�ԣ�����Ǧ����Ϊ���Դ����Al��������Pb�����������ϡ���ᣬʹ�����������Ĥ�����䷴Ӧԭ�����£�
��أ�Pb(s)��PbO2(s)��2H2SO4(aq) ===2PbSO4(s)��2H2O(l)
���أ�2Al��3H2O Al2O3��3H2���������У������ж���ȷ����
Al2O3��3H2���������У������ж���ȷ����
��� | ���� | |
A | H������Pb�缫 | H������Pb�缫 |
B | ÿ����3 molPb | ����2 molAl2O3 |
C | ������PbO2��4H����2e��===Pb2����2H2O | ������2Al��3H2O��6e��===Al2O3��6H�� |
D |
|
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У�߶���ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ӦN2(g)��3H2(g) 2NH3(g) ��H��0�Ѵﵽƽ�⣬ֻ�ı�һ��Ӱ�����أ�ƽ�ⳣ��K�뻯ѧƽ���ƶ��Ĺ�ϵ�����������
2NH3(g) ��H��0�Ѵﵽƽ�⣬ֻ�ı�һ��Ӱ�����أ�ƽ�ⳣ��K�뻯ѧƽ���ƶ��Ĺ�ϵ�����������
A��Kֵ���䣬ƽ������ƶ� B��Kֵ�仯��ƽ��һ���ƶ�
C��ƽ���ƶ���Kֵ���ܲ��� D��ƽ���ƶ���Kֵһ���仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ����У��һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ܱ�ʾ�����ӵ�������ֵ����
A��1molH2���еĵ����� B��ͨ��״���£�22.4LCO2�����ķ�����
C��0.012kg12C������ԭ���� D��1L1mol��L��1��CaCl2��Һ������Cl-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ�������ѧ���и�����ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й����У�ֻ�ƻ����Ӽ�����
A��NO2��ľ̿���� B��NaHSO4�������ۻ�
C��KHSO4��������ˮ D��Na2O2����ˮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com