
【题目】LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车电池反应为FePO4+Li![]() LiFePO4。下列有关LiFePO4电池的说法不正确的是( )
LiFePO4。下列有关LiFePO4电池的说法不正确的是( )
A.该电池充电时,阳极的电极反应式为:LiFePO4-e-=FePO4+Li+
B.该电池可用H2SO4溶液作电解质溶液
C.该电池放电时,电池内部的Li+向正极移动
D.在该电池的放电过程中,电池正极的质量逐渐增加
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】请按要求作答:
(1)请根据官能团的不同对下列有机物进行分类:
①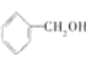 ②
②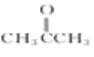 ③
③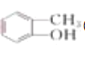 ④
④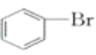 ⑤
⑤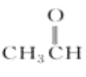 ⑥
⑥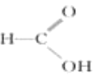 ⑦
⑦![]()
Ⅰ.醇: ________酮: ________醛: ________(填序号);
Ⅱ.④的官能团的名称为 ________,⑦的官能团的名称为 ________;
(2)分子式为 C4H8且属于烯烃的有机物的同分异构体有 ________种;
(3) ![]() 的名称为: ________;写出
的名称为: ________;写出![]() 聚合生成高分子化合物的化学方程式 ________;
聚合生成高分子化合物的化学方程式 ________;
(4) 键线式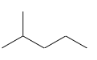 表示的有机物名称为 ________;与其互为同分异构体且一氯代物有两种的烃的结构简式________;
表示的有机物名称为 ________;与其互为同分异构体且一氯代物有两种的烃的结构简式________;
(5)篮烷分子的结构如图所示:![]()
①篮烷的分子式为: ________,其二氯代物有 ________种;
②若使 1mol 该烃的所有氢原子全部被氯原子取代,需要 ________mol 氯气。
(6)某烷烃碳架结构如图所示:![]() ,此烷烃的一溴代物有 ________种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为 ________,名称为 ________;
,此烷烃的一溴代物有 ________种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为 ________,名称为 ________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应过程中不存在电子转移的是( )
A.Zn+2HCl=ZnCl2+H2↑
B.Ca(ClO)2+2HCl=CaCl2+2HClO
C.Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O
D.3Cl2+6KOH(浓)![]() 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置电极I为Al,其他电极均为Cu,则下列说法正确的是( )
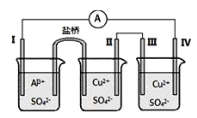
A.电流方向:电极IV→![]() →电极I
→电极I
B.电极I失电子,发生还原反应
C.电极II逐渐溶解
D.电极III的电极反应:Cu2++2e-=Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
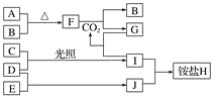
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有位于前四周期的A、B、C、D、E、F六种元素,它们的核电荷数依次增大。其中C、E、F是金属元素;A和E属同族,它们原子的最外层电子排布式为ns1。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。F元素原子共有3个价电子,其中一个价电子位于第三能层d轨道。请回答下列问题:
(1)A是_____,B是_____,F是_____。(写元素符号)
(2)写出F元素基态原子的核外价电子排布图_____,其最高化合价为_____。
(3)含E元素的化合物灼烧的颜色是_____。很多金属盐都可以发生焰色反应,其原因是_____。
(4)请写出元素C的最高价氧化物对应的水化物与HClO4反应的离子方程式:_____。
(5)C与E的金属性强弱关系是C____E,请设计一个简单实验来证明:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A含碳72.0%、含氢为6.67%,其余为氧用质谱法分析得知A的相对分子质量为150,A在光照条件下生成一溴代物B,B分子的核磁共振氢谱中有4组峰,峰面积比为2:2:2:3,B可发生如下转化关系(无机产物略):

已知:①K与氧化铁溶液发生显色反应,且环上的一元取代物只有两种结构
②当羟基与双键碳原子相连时,会发生如下转化:RCH=CHOH→RCH2CHO
请回答下列问题:
(1)B中官能团的名称是___________,反应④属于______反应类型。
(2)A的结构简式:___________。
(3)F与银氨溶液反应的离子方程式为:__________________。
(4)写出下列反应的化学方程式
反应②:________________。反应④:_______________________。
(5)N是比K多1个碳原子的同系物,同时符合下列要求的N的同分异构体有_____种。
I.苯环上有两个取代基;II.能发生水解反应;III.与氯化铁溶液发生显色反应
其中核磁共振氢谱为5组峰的为_________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)称取样品ag。
(2)将样品溶于足量稀盐酸中,过滤,滤液中主要含有___离子,滤渣中含有___;在溶解过滤时使用的仪器有___。
(3)往滤液中加入过量NaOH溶液,过滤,写出该步操作中有关的离子方程式____。
(4)在第(3)步的滤液中通入足量CO2过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧至质量不再减少为止,冷却后称量,质量为bg。有关反应的化学方程式为____。
(5)计算该样品中铝的质量分数的表达式为___。
(6)若第(3)步中加入NaOH溶液的量不足时,会使测定的结果___(“偏高”“偏低”或“无影响”,下同)。若第(4)步对沉淀的灼烧不充分时,会使测定的结果___。若第(4)步中的沉淀没有用蒸馏水洗涤时,会使测定的结果____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
碱金属及碳族元素在科研领域、生活和生产方面有广泛的应用。回答下列问题:
(1)在元素周期表中,与Li的化学性质最相似的邻族元素是__________(填元素符号),该元素基态原子最外层电子的自旋状态___________(填“相同”或“相反”)。
(2)碳和硅的有关化学键键能如下所示:
化学键 | C-H | C-O | Si-H | Si-O |
键能/kJmol-1 | 413 | 336 | 318 | 452 |
SiH4的稳定性小于CH4,更易生成氧化物,原因是__________________。
(3)天然硅酸盐都是由[SiO4]四面体以顶角氧原子相连而成,可成链状也可成环,所以硅酸盐种类繁多。下图a代表SiO44-,b、c是硅氧四面体形成的环状结构。
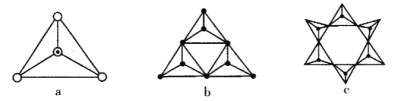
硅氧四面体中Si的轨道杂化类型为____________; 图b环状结构硅酸根的化学式为______________若在环状结构中硅的原子数为n,写出环状结构中硅酸根的通式_____________。
(4)钾与溴作用能形成溴化钾晶体,该晶体类型为___________,其晶格能可通过下图的Borm-Haber循环计算得到。
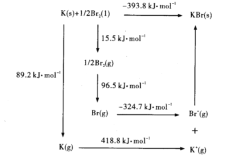
从上图可知,K原子的第一电离能为_____ kJ/mol, Br-Br键键能为______kJ/ mol,KBr的晶格能为______kJ/mol,晶格能越大,该晶体的熔点越______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com