
分析 NaClO具有强氧化性,可与浓盐酸发生氧化还原反应生成氯气,反应的离子方程式为ClO-+Cl-+2H+=Cl2+H2O,反应中只有Cl元素化合价发生变化,结合反应的化学方程式计算.
解答 解:(1)反应的化学方程式为NaClO+2HCl=Cl2+H2O+NaCl,
n(Cl2)=$\frac{1.12L}{22.4L/mol}$=0.05mol,2molHCl参加反应,只有1mol被氧化,则生成0.05mol氯气,被氧化的HCl的物质的量为0.05mol;
故答案为:0.05;
(2)由方程式可知消耗0.1molHCl,则反应后溶液中HCl的物质的量浓度为$\frac{0.05L×12mol/L-0.1mol}{0.05L}$=10.00mol/L,
故答案为:10.00.
点评 本题考查氧化还原反应的相关计算,侧重于学生的分析能力和计算能力的考查,注意把握反应的化学方程式以及化合价的变化,难度不大,注意该反应中酸的作用,为易错点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
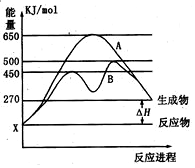 (1)已知:Fe(s)+$\frac{1}{2}$O2(g)=FeO(s),△H=-272.0KJ•mol-1
(1)已知:Fe(s)+$\frac{1}{2}$O2(g)=FeO(s),△H=-272.0KJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
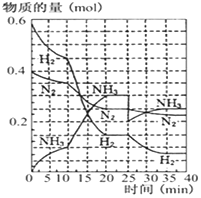 德国人发明了合成氨反应,其原理为:N2(g)+3H2(g)?2NH3(g);已知298K时,△H=-92.4kJ•mol-1,在500℃,20Mpa时,将氮气和氢气通入到体积为2升的密闭容器中,反应过程中各种物质的量变化如右图所示.
德国人发明了合成氨反应,其原理为:N2(g)+3H2(g)?2NH3(g);已知298K时,△H=-92.4kJ•mol-1,在500℃,20Mpa时,将氮气和氢气通入到体积为2升的密闭容器中,反应过程中各种物质的量变化如右图所示.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com