
| A. | 向待测溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 向待测溶液中逐滴加入氢氧化钠溶液,开始有白色沉淀生成,继续滴加氢氧化钠溶液到过量,沉淀逐渐溶解,一定有 Al3+ | |
| C. | 向待测溶液中先滴加盐酸酸化未出现沉淀,再加入 BaCl2 溶液有白色沉淀产生,一定有SO42- | |
| D. | 向待测溶液中滴加 NaOH 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,一定有NH4+ |
分析 A.碳酸根离子、碳酸氢根离子、亚硫酸根离子等均与盐酸反应生成使石灰水变浑浊的无色气体;
B.氢氧化铝、氢氧化锌、氢氧化铍均溶于NaOH溶液;
C.先滴加稀盐酸,排除其它离子的干扰;
D.铵根离子与碱反应生成氨气,氨气可使湿润的红色石蕊试纸变蓝.
解答 解:A.碳酸根离子、碳酸氢根离子、亚硫酸根离子等均与盐酸反应生成使石灰水变浑浊的无色气体,则向待测溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,可能有CO32-或SO32-等,故A错误;
B.氢氧化铝、氢氧化锌、氢氧化铍均溶于NaOH溶液,则向待测溶液中逐滴加入氢氧化钠溶液,开始有白色沉淀生成,继续滴加氢氧化钠溶液到过量,沉淀逐渐溶解,可能有 Al3+,故B错误;
C.先滴加稀盐酸,排除其它离子的干扰,再滴加BaCl2溶液后出现白色沉淀,可说明溶液中一定含有SO42-,故C正确;
D.铵根离子与碱反应生成氨气,氨气可使湿润的红色石蕊试纸变蓝,则向待测溶液中滴加 NaOH 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,一定有NH4+,故的正确;
故选CD.
点评 本题考查常见离子的检验,为高频考点,把握离子检验中排除干扰离子、试剂与现象、结论的关系等为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H2作氧化剂 | B. | 铜元素化合价升高 | ||
| C. | 氢元素化合价降低 | D. | Cu是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对燃烧现象的深入研究 | B. | 对空气组成的研究 | ||
| C. | 用原子--分子论来研究化学反应后 | D. | 英国科学家汤姆生发现电子后 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质 Cl2、Br2、I2的氧化性强弱 | |
| B. | 气态氢化物 NH3、H2O、HF 的稳定性 | |
| C. | 碱金属单质 Li、Na、K 与水反应的剧烈程度 | |
| D. | 1mol Na、Mg、Al 分别与足量盐酸反应时失电子数的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同主族金属的原子半径越大熔点越高 | |
| B. | 稀有气体原子序数越大沸点越高 | |
| C. | 同周期元素的原子半径越小越易失去电子 | |
| D. | 在晶体中只要有阳离子就一定有阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了保持腊肉肉质鲜美,添加过量的亚硝酸钠 | |
| B. | 为了防止食用鱿鱼变质,用甲醛水溶液浸泡存放 | |
| C. | 为了防止黄曲霉素对人体的危害,绝对不能食用霉变食物 | |
| D. | 为了防止摄入锌不足引起疾病,过量服用补锌药剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
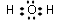 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com