
【题目】有关物质的转化关系如图所示(反应条件及部分产物已略去)。A、C、D中均含有相同的非金属元素,C、G为气体,D为淡黄色单质,I为常见强酸,反应③为化合反应。J溶液与KSCN溶液混合呈血红色。A中仅含两种元素,且元素质量比为7:8。

请回答下列问题:
(1)A的化学式为__________。
(2)H的电子式为__________。
(3)写出①的离子方程式为__________。
(4)写出②的化学方程式为____________并用单线桥标出电子转移方向和数目。
【答案】 FeS2 ![]() FeS2+2H+==Fe2++S+H2S↑
FeS2+2H+==Fe2++S+H2S↑ ![]()
【解析】J溶液与KSCN溶液混合呈血红色,J溶液中含有铁离子;D为淡黄色单质,D为硫;A中仅含两种元素,则A中含有硫和铁2种元素,元素质量比为7:8,则原子个数比为![]() :
:![]() =
=![]() 或
或![]() :
:![]() =
=![]() (不合理),则A的化学式为FeS2;A与浓盐酸反应生成BCD,D为S,则-1价的S发生歧化反应,C为气体,则C为H2S,根据元素守恒,B为氯化亚铁,与氢氧化钠溶液反应生成E(氢氧化亚铁),E在足量空气中被氧化生成F(氢氧化铁);D与I的浓溶液反应生成G,G为气体,则G为SO2,I为浓硫酸,反应③为化合反应则H为双氧水,J为硫酸铁。
(不合理),则A的化学式为FeS2;A与浓盐酸反应生成BCD,D为S,则-1价的S发生歧化反应,C为气体,则C为H2S,根据元素守恒,B为氯化亚铁,与氢氧化钠溶液反应生成E(氢氧化亚铁),E在足量空气中被氧化生成F(氢氧化铁);D与I的浓溶液反应生成G,G为气体,则G为SO2,I为浓硫酸,反应③为化合反应则H为双氧水,J为硫酸铁。
(1)根据上述分析,A的化学式为FeS2,故答案为:FeS2;
(2)H为双氧水,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)反应①的离子方程式为FeS2+2H+==Fe2++S+H2S↑,故答案为:FeS2+2H+==Fe2++S+H2S↑;
(4)反应②的化学方程式为S+2H2SO4![]() 3SO2↑+2H2O,电子转移方向和数目用单线桥表示为
3SO2↑+2H2O,电子转移方向和数目用单线桥表示为![]() ,故答案为:
,故答案为:![]() 。
。


 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是( )

A. 由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方 程式为:MgBr2(s)+Cl2(g)![]() MgCl2(s)+Br2(g) ΔH=+117 kJ·mol-1
MgCl2(s)+Br2(g) ΔH=+117 kJ·mol-1
B. 热稳定性: MgI2 > MgBr2 > MgCl2 > MgF2
C. 工业上可由电解MgCl2溶液冶炼金属Mg,该过程需吸收热量
D. 金属镁和卤素单质(X2)的反应能自发进行是因为ΔH均小于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是( )
A. 含有4molHCl的浓盐酸与足量MnO2反应,生成1molCl2
B. 78g Na2O2与足量水充分反应时电子转移数为2NA
C. 标准状况下,22.4L SO3中所含的SO3分子数为NA
D. 常温常压下,8g O2所含的质子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件下,两瓶气体所含的原子数一定相等的是
①同质量、不同密度的Cl2和CO ②同温度、同体积的H2和 N2
③同体积、同密度的 C2H4和C3H6两种气体④同压强、同体积的 N2和 CO两种气体.
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是

A. 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液不褪色
B. 若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C. 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色
D. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向一带活塞的密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图所示。下列对t1时刻改变条件的推断正确的是( )
2SO3(g) ΔH<0。达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图所示。下列对t1时刻改变条件的推断正确的是( )
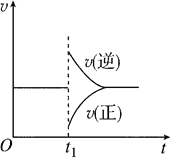
A. 保持压强不变,升高反应温度
B. 保持温度不变,增大容器体积
C. 保持温度和容器体积不变,充入1 mol SO3(g)
D. 保持温度和压强不变,充入1 mol SO3(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列叙述正确的是
A. 若V1L pH=11的NaOH溶液与V2 L pH=3的HA溶液混合后显中性,则V1≤V2
B. 等体积、等物质的量浓度的NaCl溶液中离子总数大于NaClO溶液中离子总数
C. 等体积、等物质的量浓度的Na2CO3和NaHCO3溶液混合:![]() <
<![]()
D. 将CH3COOH溶液与NaOH溶液混合,若混合后的溶液中c(CH3COO-)+c(CH3COOH)=2c(Na+),则c(OH-)+c(CH3COO-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常采用高锰酸钾加热分解法制取氧气,某兴趣小组经查阅资料获知:制得氧气后固体残余物中的锰酸钾(K2MnO4)具有强氧化性,与还原剂、有机物、易燃物混合可形成爆炸性混合物,如不妥善处置将造成危险。因此该小组对该残余物进行分离提纯,得到锰酸钾晶体,利用回收的锰酸钾与浓盐酸反应制取氯气,并设计实验验证氯气化学性质。

(1)检验该套装置气密性的方法是:______________________________;
(2)打开分液漏斗活塞及弹簧夹2,观察到烧瓶壁有紫红色物质生成并逐渐消失,黄绿色气体充满烧瓶。反应结束后,烧瓶内有黑色固体残余,写出过程中发生的化学反应方程式:_________________________________________;
(3)该方法制取氯气比用纯净的高锰酸钾要缓和平稳许多,试分析原因:________;
(4)该小组利用装置C吸收氯气制备漂白粉。
①C中盛装的试剂为:________________________________;(写名称)
②陶瓷多孔球泡的作用是:_________________________________________________;
(5)测定漂白粉有效成分的质量分数:称取1.5g所制漂白粉配成溶液,调节pH值并加入指示剂,用0.1000mol/L KI溶液进行滴定,三次平行实验平均每次消耗20.00mL标准液时达到滴定终点。已知氧化性:ClO-> IO3-> I2
①所选的指示剂为:______________,到达滴定终点的标志是:______________________;
②该漂白粉中有效成分的质量分数为:__________________________。
(6)打开分液漏斗活塞及弹簧夹1,可观察到D中的现象为:______________;该现象能够证明氯气有氧化性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外实验小组从煤油中取出一块钠,用滤纸吸净其表面的煤油,用切刀切下数块,分别进行实验研究:
(1)切下的钠块表面变暗,其反应的化学方程式为________________。
(2)将一小块金属钠投入水中,发生反应的离子方程式为 ____________________;可观察到的实验现象是____________(填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)将其中一块钠放入坩埚中加热,反应现象为: ______________________________,反应的化学方程式是________________________。
(4)过氧化钠是钠的一种重要化合物,其中一种用途是用于呼吸面具或潜水艇中氧气的来源,涉及的主要反应的化学方程式为_______________(写一个即可),若15.6gNa2O2参加反应,则最多可制得标准状况下氧气的体积为________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com