
下列离子在指定溶液中一定能大量共存的是
A.能使甲基橙变红的溶液中:Fe2+、Al3+、NO3-、Cl-、S2-
B.在pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
C.室温下,由水电离的c(H+)=10-10mol/L的溶液中:Cl-、HCO3-、NO3-、NH4+、F-
D.加入Mg能放出H2的溶液中:Mg2+、NH4+、ClO-、K+、SO42-
B
【解析】
试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A.能使甲基橙变红的溶液显酸性,在酸性溶液中硝酸根能氧化Fe2+与S2-,不能大量共存,A错误;B.pH=11的溶液显碱性,则Na+、AlO2—、NO3—、S2-、SO32—之间不反应,可以大量共存,B正确;C.室温下,由水电离的c(H+)=10-10mol/L的溶液中水的电离被抑制,溶液可能显酸性,也可能显碱性,如果显酸性,则碳酸氢根、氟离子不能大量共存。如果显碱性,则碳酸氢根与铵根离子均不能大量共存,C错误;D.加入Mg能放出H2的溶液显酸性,则ClO-不能大量共存,D错误,答案选B。
考点:考查离子共存判断


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源:2014-2015学年湖北省荆州市部分县市高三上学期期末统考理综化学试卷(解析版) 题型:选择题
某澄清透明溶液中只可能含有①Al3+,②Mg2+,③Fe3+,④Fe2+,⑤H+,⑥CO32-, ⑦NO3- 中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示。则该溶液中一定含有的离子是
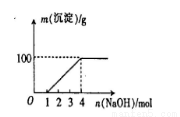
A.②⑤⑥⑦ B.②③⑤⑦
C.①②③⑥⑦ D.①②③④⑤⑦
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:选择题
将反应Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是
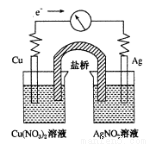
A.KNO3盐桥中的K+移向Cu(NO3)2溶液
B.Ag作负极,Cu作正极
C.工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大
D.取出盐桥后,电流计的指针依然发生偏转
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通人 SO2气体,溶液逐渐变成无色。下列分析正确的是
A.滴加KI溶液时,转移2 mol e-时生成 1 mol白色沉淀
B.通入SO2后溶液逐渐变成无色,体现了 SO2的漂白性
C.通入SO2时,SO2与I2反应,I2作还原剂
D.上述实验条件下,物质的氧化性:Cu2+ >I2 > SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
下图所示与对应叙述相符的是
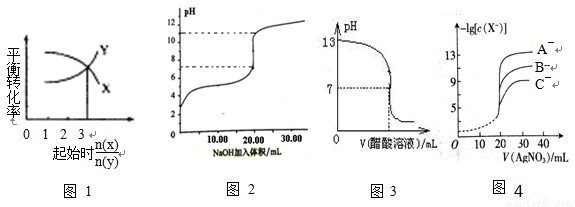
A.一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X + 3Y Z
Z
B.图2表示NaOH溶液滴加到0.1 mol/L的一元酸溶液得到的滴定曲线(常温下),该实验最好选取酚酞作指示剂
C.常温下,向NaOH溶液中逐滴加入等浓度的醋酸溶液,所得滴定曲线如图3所示。当7<pH<13 时,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图4可确定首先沉淀的是C-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,2.24 L SO3含有分子的数目为0.1NA
B.1 mol O2与Na完全反应,转移电子数一定为4NA
C.常温常压下,1.6 g CH4中含有共价键的数目为0.4NA
D.将2 mL 0.5 mol/L硅酸钠溶液滴入盐酸中制得硅酸胶体,所含胶粒数目为0.001NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:实验题
(11分)果汁在生产过程中添加亚硫酸及其盐类,以抑制有害微生物的生长及抗氧化。某化学兴趣小组查阅文献后,用下图所示装置测定某果汁样品中SO2残留量。
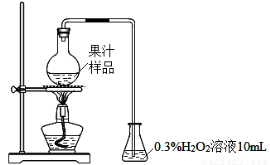
实验步骤:
(ⅰ)在烧瓶中加入50.00 mL果汁样品与3mL浓硫酸的混合液,加热10 min。
(ⅱ)移出锥形瓶,迅速滴入2~3滴酚酞试液,用0.01000 mol·L-1NaOH标准溶液滴定。
回答问题:
(1)实验室配制NaOH标准溶液时,不需要用到的仪器是 。
A.容量瓶 B.胶头滴管 C.烧瓶 D.玻璃棒
(2)将50. 00 mL果汁样品与3mL浓硫酸混合的操作是 。
(3)锥形瓶中发生反应的离子方程式是 。
(4)若步骤(ⅱ)消耗NaOH标准溶液25. 00 mL,则果汁样品中SO2残留量是 g/L。
(5)若改用0.5%的碘水10 mL作吸收液,实验中消耗NaOH标准溶液体积 。
A.V = 25 mL B.25 mL<V<50 mL C.V>50 mL
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高一上学期期末考试化学(B)试卷(解析版) 题型:填空题
向含2 mol H2SO4和1 mol HNO3的混合稀溶液中加入过量的锌,假设HNO3被还原的产物全部为NO。
①写出反应的离子方程式 。
②生成的气体在标况下的体积为: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省荆门市高一上学期期末考试化学试卷(解析版) 题型:计算题
把5.1g镁铝合金的粉末放入500mL1mol·L-1盐酸中,恰好完全反应。试计算:
(1)该合金中镁和铝的物质的量。
(2)将等质量的该合金投入到足量的氢氧化钠溶液中,求标况下放出气体的体积。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com