
����Ŀ����1����һ��������N2��H2��Ӧ����NH3����ش�
������Ӧ���������ΪE1���������������ΪE2����E1��E2����÷�ӦΪ________(����ȡ����ȡ�)��Ӧ��
����֪��1molH��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ___________________________________________��
��2��ʵ������50mL0.50mol��L��1������50mLijŨ�ȵ�NaOH��Һ����ͼ��ʾװ���з�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ���װ�����������ԵĴ�������һ����ȱ��һ�ֲ���������������������Ϊ___________________________��ʵ�����ṩ��0.50mol��L��1��0.55mol��L��1����Ũ�ȵ�NaOH��Һ��Ӧѡ��___________mol��L��1��NaOH��Һ����ʵ�顣

��3������������CO2���ڻ��ۣ���в����̬����������������ܵ�ȫ�����ע����ҵ�ϳ��ø�Ũ�ȵ�K2CO3��Һ����CO2������ҺX�������õ�ⷨʹK2CO3��Һ��������װ��ʾ��ͼ���£�

���������������ķ�Ӧ����__________________________________��H����HCO===H2O��CO2����
�ڼ���CO![]() ��������������ԭ����____________________________________��
��������������ԭ����____________________________________��
��4�������£���NaOH��Һ����SO2�õ�pH��9��Na2SO3��Һ���Լ�����Һ��![]() ��_______����������H2SO3�ĵ���ƽ�ⳣ��Ka1��1.0��10��2��Ka2��6.0��10��8��
��_______����������H2SO3�ĵ���ƽ�ⳣ��Ka1��1.0��10��2��Ka2��6.0��10��8��
���𰸡� ���� N2(g)��3H2(g)![]() 2NH3(g)����H����92kJ��mol��1 ���β�������� 0.55 4OH����4e��===2H2O��O2�� HCO���ڵ���ƽ�⣺HCO
2NH3(g)����H����92kJ��mol��1 ���β�������� 0.55 4OH����4e��===2H2O��O2�� HCO���ڵ���ƽ�⣺HCO![]() H����CO
H����CO![]() ������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO
������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO![]() ����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO
����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO![]() ��CO
��CO![]() ����) 60
����) 60
�������� (1)����Ӧ��������������������������Ϊ���ȷ�Ӧ��
����ѧ��Ӧ������ѧ�����������������γ��»�ѧ���ų����������ݷ���ʽ����ֱ����պͷų����������Դ˼��㷴Ӧ�Ȳ��ж����Ȼ��Ƿ�����
(2)�������ȼƵĹ������жϸ�װ�õ�ȱ��������Ϊ��ʹ��Ӧ���,NaOHӦ������
��3�������������������ӷŵ�����������
��̼��������ӳ̶ȵ���ƽ�⡢���������Ӻ�̼��������ӷ�Ӧ����̼���������
��4������Ka2=![]() ������Һ��
������Һ��![]() =
=![]() ���Դ˽����
���Դ˽����
���:(1)�ٷ�Ӧ���������ΪE1���������������ΪE2����E1>E2����÷�ӦΪ���ȷ�Ӧ��
��ˣ�������ȷ������������
���ڷ�ӦN2+3H22NH3��������3molH��H����1molN��N�����յ�����Ϊ:3��436 kJ+946 kJ=2254 kJ������2mol NH3�����γ�6mol1molN��H�����ų�������Ϊ:6��391kJ=2346kJ�����յ�������,�ų���������,�÷�ӦΪ���ȷ�Ӧ,�ų�������Ϊ��2346kJ -2254 kJ =92kJ��
��ˣ�������ȷ������N2(g)��3H2(g)![]() 2NH3(g)����H����92kJ��mol��1 ��
2NH3(g)����H����92kJ��mol��1 ��
(2)�������ȼƵĹ������֪����װ�õ�ȱ�������ǻ��β����������ʵ�����ṩ��0.50mol��L��1��0.55mol��L��1����Ũ�ȵ�NaOH��Һ��Ϊ��ʹ��Ӧ���,NaOHӦ����,����ѡ��0.55mol��L��1����Һ����ʵ����
��ˣ�������ȷ���������β����������0.55��
(3) �����������������ӷŵ�����������ˮ,�缫��ӦʽΪ4OH����4e��===2H2O��O2����
��ˣ�������ȷ������4OH����4e��===2H2O��O2����
��HCO���ڵ���ƽ�⣺HCO![]() H����CO
H����CO![]() ������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO
������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO![]() ����������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO
����������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO![]() ��CO
��CO![]() ������
������
��ˣ�������ȷ������HCO���ڵ���ƽ�⣺HCO![]() H����CO
H����CO![]() ������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO
������H���ŵ�Ũ�ȼ�Сƽ�����ƣ�CO![]() ����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO
����(������H���ŵ�OH��Ũ������OH����HCO��Ӧ����CO![]() ��CO
��CO![]() ����)��
����)��
��4��pH=9����Һ��c��H+��=10-9mol/L������Ka2=![]() ������Һ��
������Һ��![]() =
=![]() ��=
��=![]() =60��
=60��
�ʴ�Ϊ��60��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧΪ̽��Ԫ�����ڱ���Ԫ�����ʵĵݱ���ɣ����������ʵ�顣
����(1)���ơ��ء�þ������1mol�ֱ�Ͷ�뵽������ͬŨ�ȵ������У���Ԥ��ʵ������_____�����ᷴӦ����ң�______�����ᷴӦ������������ࡣ
(2)��Na2S��Һ��ͨ���������ֻ�ɫ���ǣ���֤��Cl�ķǽ����Ա�Sǿ����Ӧ�����ӷ���ʽΪ_______________________________________________________��
(3)д��������ĵ���ʽ____________��
����������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯����
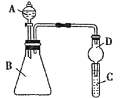
(1)����D������Ϊ_________________________________________��
(2)��Ҫ֤���ǽ����ԣ�Cl��I����A�м�Ũ���ᣬB�м�KMnO4��C�мӵ��۵⻯�ػ����Һ���۲쵽C����Һ_______(������)������֤�����ӻ��������Ĺ۵㿼�ǣ���װ��ȱ��β������װ�ã������ӷ���ʽ��ʾ��β������ԭ��______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȳ�����Ũ�������ֲ����ü�ʯ�Ҹ���������ǣ� ��
A.Cl2B.H2SC.SO2D.CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.���ͳ�����ʻ�����У���������ת��Ϊ��ѧ�ܣ���ѧ����ת��Ϊ����
B.ըҩ������ըʱ��ѧ����ȫת��Ϊ����
C.̿ȼ��ʱ��ѧ����Ҫת��Ϊ����
D.���ȼ��ʱ�����ֻ�ѧ��ת��Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л���������ж���ȷ����(����)
A.�л������ﶼ�Ǵ��л�������ȡ���������
B.�л������ﶼ��ȼ��
C.�л������ﲻһ����������ˮ
D.�л������ﲻ�߱��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����̿�(��Ҫ�ɷ�ΪMnO2)�������Ʊ��̼��仯����ִ�ұ�������̵Ĺ�����������ͼ��ʾ������������������һ������

�±�Ϊt��ʱ���й����ʵ�Ksp
���� | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
Ksp | 4.0��10-38 | 2.2 | 5.5 | 1.9 | 6.3 | 9.1 | 2.5 | 2.2 |
���̿�ԭ�����ķ�ӦΪ��12MnO2��C6H12O6��12H2SO4===12MnSO4��6CO2����18H2O
��1��д��һ�������ԭ�������ʵĴ�ʩ��_________________________
��2������pH ���������ɵij���Ϊ________������MnF2����ҪĿ���dz�ȥ__________ (�Ca2��������Fe3������Cu2����)
��3����Ũ�ȵģ�NH4)2S�루N4)2SO4 ��Һ�У�NH4����Ũ�ȴ�СΪ��ǰ��________���ߣ������������ �� ��=�� )��
��4����MnSO4��ȡMnCO3��MnSO4��Һ�м���(NH4)2CO3��Һ����MnCO3��ͬʱ�������Mn(OH)2�����ܵ�ԭ���У�MnCO3(s)��2OH��(aq)![]() Mn(OH)2(s)��CO
Mn(OH)2(s)��CO![]() (aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K��_________________(����һλС��)��
(aq)��t��ʱ������÷�Ӧ��ƽ�ⳣ��K��_________________(����һλС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A. ��״���£�11.2LSO2�����к���ԭ��������18gˮ�к��е���ԭ����
B. 5.6 g��������ϡ���ᷴӦʧȥ�ĵ��ӵ����ʵ���Ϊ0.3 mol
C. 100g98%��Ũ������������ԭ�Ӹ���Ϊ4mol
D. 20gNaOH����1Lˮ��������Һ��c(Na+)=0.5mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���ѧ����������ᡢ����������أ����������в���ȷ���ǣ� ��
A.�����������˱ȳ���������
B.����й©��Ӧ˳����ʹ���
C.����ȼúʹ�ã������ڽ��Ϳ�����PM2.5����
D.��������Ͷ�����������Ҫ�Ĵ�����Ⱦ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�(CH3OH)����Ҫ���ܼ������ȼ�ϣ���ҵ�ϳ���CO��H2�Ļ������Ϊԭ����һ���������Ʊ��״���
(1)��ҵ�Ͽ���ͨ������;�����H2�����н���Ч����õ���___________��
A.���·ֽ�ˮ��ȡH2:2H2O![]() 2H2��+O2��
2H2��+O2��
B.���ˮ��ȡH2:2 H2O![]() 2H2��+ O2��
2H2��+ O2��
C.������ˮ��Ӧ��ȡH2:CH4+ H2O![]() 3H2+CO
3H2+CO
D.�ڹ���������£�����̫���ֽܷ�ˮ��ȡH2:2H2O![]() 2H2��+ O2��
2H2��+ O2��
(2)��2L���ܱ������г���1mo1 CO��2mol H2��һ�������·�����Ӧ;CO(g)+2H2(g) ![]() CH3OH(g)�����CO��CH3OH(g)�����ʵ�����ʱ��ı仯����ͼ��ʾ��
CH3OH(g)�����CO��CH3OH(g)�����ʵ�����ʱ��ı仯����ͼ��ʾ��
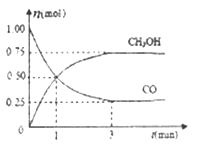
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)=_____��ƽ��ʱ�������������Ϊ____��
���ܹ��жϸ÷�Ӧ�ﵽƽ�����______��
A. CO��H2��CH3OH�������ʵ�Ũ�����
B. �ܱ������л��������ܶȲ��ٸı�
C. �ܱ������л�������ƽ����Է����������ٸı�
D. ��ͬʱ��������1mo1CO��ͬʱ����1mol CH3OH
(3)Ϊʹ�ϳɼ״�ԭ�ϵ�ԭ�������ʴﵽ100%��ʵ���������Ʊ�ˮú��ʱ����ʹ��CH4��������Ͷ��ʱ��n(C):n(H2O):n(CH4)=__________��
(4)�ݱ��������Ħ��������˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ����������������غ�﮵�ص�10����������ʹ��һ���²ų��һ�Ρ��ٶ��ŵ�����У��״���ȫ���������Ķ�����̼�������������CO32-����õ�ظ����ĵ缫��ӦʽΪ__________________����طŵ��������Һ��pH��_____(�����½�����������������������)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com