
【题目】NA为阿伏伽德罗常数,下列叙述错误的是( )
A. 18g H2O中含的质子数为10NA
B. 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
C. 46g NO2和N2O4混合气体中含有原子总数为3NA
D. 12g金刚石含有的共价键数为4NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】苏合香醇可以用作食用香精,其结构简式如图所示。
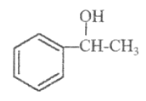
(1)苏合香醇的分子式为_____________,它不能发生的有机反应类型有(填数字序号)_____________。
①取代反应 ②加成反应 ③消去反应 ④加聚反应 ⑤氧化反应 ⑥水解反应
(2)有机物丙是一种香料,其合成路线如图。其中A为烃,相对分子质量为56;甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物。
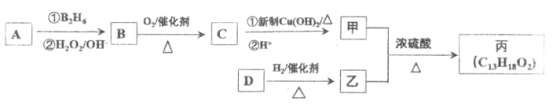
已知:R-CH=CH2 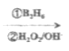 R-CH2CH2OH
R-CH2CH2OH
①A的结构简式是_____________。
②写出由B到C的化学反应方程式_____________。
③写出C与新制氢氧化铜悬浊液反应的化学反应方程式_____________。
④B的同分异构体能与钠反应生成氢气,不能发生催化氧化反应,其结构简式_____________。
⑤丙中含有两个—CH3,则甲与乙反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。提取碘的途径如下图所示,下列有关叙述正确的是
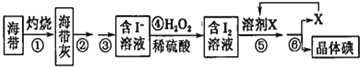
A.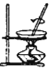 此装置进行操作①
此装置进行操作①
B.②③操作中所用到的玻璃仪器有:玻璃棒、烧杯、分液漏斗
C.④中当1molH2O2氧化I-时,转移电子数为2NA
D.溶剂X可选用酒精或苯
查看答案和解析>>
科目:高中化学 来源: 题型:
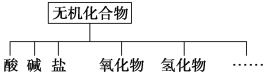
【题目】无机化合物可根据其组成和性质进行分类。
(1)如图所示的物质分类方法的名称是______________。
(2)
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②______ | ③________ ④Ba(OH)2 | ⑤Na2CO3 ⑥_______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥后面。
(3)写出⑦转化为⑤的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2.4gRSO4中含0.02molR2+,则RSO4的摩尔质量是____;R的相对原子质量约是___。
(2)除去下列物质中所混有的少量杂质,指明应加入的试剂,写出有关的离子方程式。
NaHCO3溶液(Na2CO3):试剂_________,离子方程式:___________。
(3)实验室需要0.1mol/L的硫酸980mL,欲用密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸进行配制,则需用量筒量取______mL进行配制。假如其他操作均准确无误,若使用量筒量取时俯视读数,最终所配溶液的浓度________(选填“偏高”、“偏低”或“无影响”);若溶解时未冷却,直接转移到容量瓶中至刻度线,最终所配溶液的浓度_________(选填“偏高”、“偏低”或“无影响”)。
(4)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是__。反应化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HX的酸性比HY弱,在物质的量浓度均为0.1molL﹣1的NaX和NaY混合溶液中,下列排序正确的是( )
A. c(OH﹣)>c(HX)>c(HY)>c(H+)
B. c(OH﹣)>c(X﹣)>c(Y﹣)>c(H+)
C. c(OH﹣)>c(Y﹣)>c(X﹣)>c(H+)
D. c(OH﹣)>c(HY)>c(HX)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是( )
A.向硫酸铁溶液中加入过量铁粉:Fe+2Fe3+=3Fe2+
B.向Na2CO3溶液中滴加稀盐酸:Na2CO3+2H+=2Na++CO2↑+H2O
C.向铜粉中加入稀硫酸:Cu+2H+=Cu2++H2↑
D.向铝粉中加入足量NaOH溶液:2Al+2OH-=2AlO![]() +H2↑
+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下列物质
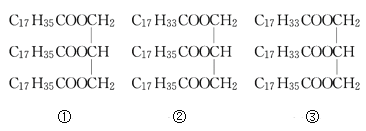
(1)属于简单甘油酯的是(填序号,下同)____,属于混合甘油酯的是______。
(2)①发生皂化反应的化学方程式为________。
Ⅱ.完成银镜反应实验:在AgNO3溶液中逐滴加入氨水,开始时在AgNO3溶液中出现白色沉淀,反应的离子方程式为_____,继续滴入氨水至沉淀溶解,反应的化学方程式为____,边滴边振荡直滴到______为止。再加入乙醛溶液后,水浴加热现象是____,化学方程式为:______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类非常重要的反应。回答下列问题:
(1)按如图所示操作,充分反应后:
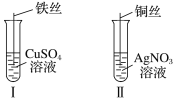
①Ⅰ中发生反应的离子方程式为__________________________________;
②Ⅱ中铜丝上观察到的现象是___________________________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。其中氧化产物是________
(3)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有_______(填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为________________________________________________
(5)写出氢气还原氧化铜反应的化学方程式,并用双线桥法表示电子转移的方向和数目。________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com