
| Ag��22.4L |
| 46g |
| A��22.4 |
| 46 |
| A��22.4 |
| 24 |
| A��67.2 |
| 54 |
| A��22.4 |
| 46 |
| A��22.4 |
| 24 |
| A��67.2 |
| 54 |
| 1 |
| 23 |
| 1 |
| 12 |
| 1 |
| 9 |
| 1 |
| 23 |
| 1 |
| 12 |
| 1 |
| 9 |
| 1 |
| 2 |
| 3 |
| 2 |
| 3.36L |
| 22.4L/mol |
| 2 |
| 3 |
| x |
| 0.15 |


 һ����������ϵ�д�
һ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��m=n | B��m��n |
| C��m��n | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڢۢ� | B���٢ۢ� |
| C���٢ڢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��450 mL��52.7 g |
| B��500 mL��58.5 g |
| C��1000 mL��117 g |
| D��������111.2 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ܶȱ�Ϊ16��11 |
| B���ܶȱ�Ϊ11��16 |
| C�������Ϊ16��11 |
| D��ԭ������Ϊ1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�22.4LH2O���еķ�����Ϊ NA |
| B�����³�ѹ�£�1.06g Na2CO3���е�Na+������Ϊ0.02 NA |
| C��ͨ��״���£�NA ��CO2����ռ�е����Ϊ22.4L |
| D�����ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl- ����Ϊ NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ӻϳ��������Ļ�����壬NH3�ĺ�����С�������������Ĺ�����Ч�ʶ��ܵ� |
| B�����ڰ���Һ�����������N2��H2��ʵ��������ѭ��ʹ�ã�����������˵���IJ��ʺܸ� |
| C���ϳɰ���ҵ�ķ�Ӧ�¶ȿ�����500�棬Ŀ����ʹ��ѧƽ��������Ӧ�����ƶ� |
| D���ϳɰ������õ�ѹǿ��20 MPa��50 MPa�����ڸ�ѹǿ������ý�Ļ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
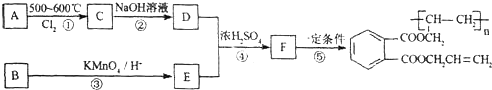
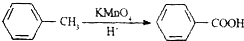
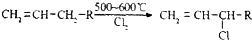
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com