
 ¹ż¶ÉŌŖĖŲĢśæÉŠĪ³É¶ąÖÖÅäŗĻĪļ£¬Čē£ŗ[Fe£ØCN£©6]4-”¢Fe£ØSCN£©3µČ£®
¹ż¶ÉŌŖĖŲĢśæÉŠĪ³É¶ąÖÖÅäŗĻĪļ£¬Čē£ŗ[Fe£ØCN£©6]4-”¢Fe£ØSCN£©3µČ£®·ÖĪö £Ø1£©øł¾ŻĢśµÄŌ×ÓŠņŹżĪŖ26£¬½įŗĻÄÜĮæ×īµĶŌĄķŹéŠ“»łĢ¬Ō×ӵĵē×ÓÅŲ¼Ź½£»
£Ø2£©Ķ¬Ņ»ÖÜĘŚŌŖĖŲµÄµŚŅ»µēĄėÄÜĖę×ÅŌ×ÓŠņŹżµÄŌö“ó¶ų³ŹŌö“óµÄĒ÷ŹĘ£¬µ«µŚIIA×åŗĶµŚVA×åŌŖĖŲµÄµŚŅ»µēĄėÄÜ“óÓŚĻąĮŚŌŖĖŲ£»
£Ø3£©Ō×ÓøöŹżĻąµČĒŅ¼Ūµē×ÓŹżĻąµČµÄ·Ö×Ó»ņĄė×ÓĪŖµČµē×ÓĢ壻1molFe£ØCN£©63-ÖŠCNŗ¬ÓŠC”¢NČż¼ü£¬ĘäÖŠ1øöŹĒ¦Ņ¼ü£¬NŌ×ÓÓŠ¹Ā¶Ōµē×Ó£¬ĢśŌ×ÓÓŠæÕ¹ģµĄ£¬ĖłŅŌĆæøöĢśĄė×ÓÓėCN-ŠĪ³É4øöÅäĪ»¼ü£¬ĖłŅŌ¹²ÓĆ6øö¦Ņ¼ü£¬1molFe£ØCN£©63-ÖŠŗ¬ÓŠ¦Ņ¼üŹżĪŖ12mol£»
£Ø4£©ŅĄ¾ŻFe£ØCO£©5µÄČŪ·ŠµćµĶ£¬ĒŅŅ×ČÜÓŚĖÄĀČ»ÆĢ¼ÅŠ¶Ļ¾§ĢåĄąŠĶ£»
£Ø5£©ŅĄ¾ŻÕż·½ĢåÖŠ£¬¶„µćÉĻµÄŌ×Ó±»8øö¾§°ūÕ¼ÓŠ£¬ĢåŠÄÉĻµÄŌ×Ó±»1øö¾§°ūÕ¼ÓŠ£¬ĢśĀĮŗĻ½š¾§°ū½į¹¹ĀĮŌ×ӵďżÄæĪŖ4”Į$\frac{1}{8}$=$\frac{1}{2}$£»ĢśŌ×ÓŹżÄæĪŖ1+4”Į$\frac{1}{8}$=$\frac{3}{2}$£¬ĖłŅŌĀĮŌ×ÓÓėĢśŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ3£®
½ā“š ½ā£ŗ£Ø1£©ĢśµÄŌ×ÓŠņŹżĪŖ26£¬øł¾ŻÄÜĮæ×īµĶŌĄķĘäĢ¬Ō×ӵĵē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d64s2»ņ[Ar]3d64s2£¬
¹Ź“š°øĪŖ£ŗ1s22s22p63s23p63d64s2»ņ[Ar]3d64s2£»
£Ø2£©Ķ¬ÖÜĘŚµŚŅ»µēĄėÄÜ×Ō×ó¶ųÓŅ¾ßÓŠŌö“óĒ÷ŹĘ£¬ĖłŅŌµŚŅ»µēĄėÄÜO£¾C£®ÓÉÓŚµŖŌŖĖŲŌ×Ó2pÄܼ¶ÓŠ3øöµē×Ó£¬“¦ÓŚ°ėĀśĪȶØדĢ¬£¬ÄÜĮæ½ĻµĶ£¬µŚŅ»µēĄėÄÜ“óÓŚĻąĮŚŌŖĖŲ£¬ĖłŅŌC”¢N”¢OČżÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņŹĒN£¾O£¾C£¬
¹Ź“š°øĪŖ£ŗN£¾O£¾C£»
£Ø3£©CN-ŗ¬ÓŠ2øöŌ×Ó£¬¼Ūµē×Ó×ÜŹżĪŖ4+5+1=10£¬¹ŹĘäµČµē×ÓĢåĪŖµŖĘų·Ö×Ó”¢COµČ£¬1molFe£ØCN£©63-ÖŠCNŗ¬ÓŠC”¢NČż¼ü£¬ĘäÖŠ1øöŹĒ¦Ņ¼ü£¬NŌ×ÓÓŠ¹Ā¶Ōµē×Ó£¬ĢśŌ×ÓÓŠæÕ¹ģµĄ£¬ĖłŅŌĆæøöCN-ÓėĢśĄė×ÓŠĪ³É6øöÅäĪ»¼ü£¬ĖłŅŌ¹²ÓĆ12øö¦Ņ¼ü£¬1molFe£ØCN£©32-ÖŠŗ¬ÓŠ¦Ņ¼üŹżĪŖ12mol£¬øöŹżĪŖ£ŗ12NA£¬
¹Ź“š°øĪŖ£ŗCO»ņN2£»12”Į6.02”Į1023øö»ņ12NA£»
£Ø4£©Fe£ØCO£©3µÄČŪ·ŠµćµĶ£¬ĒŅŅ×ČÜÓŚĖÄĀČ»ÆĢ¼£¬ŅĄ¾Ż·Ö×Ó¾§ĢåČŪ·ŠµćµĶ£¬ĒŅ“ęŌŚĻąĖĘĻąČÜŌĄķ£¬æÉÖŖFe£ØCO£©3ĪŖ·Ö×Ó¾§Ģ壬
¹Ź“š°øĪŖ£ŗ·Ö×Ó¾§Ģ壻
£Ø5£©ŅĄ¾ŻĢśĀĮŗĻ½š¾§°ū½į¹¹ĀĮŌ×ӵďżÄæĪŖ4”Į$\frac{1}{8}$=$\frac{1}{2}$£»ĢśŌ×ÓŹżÄæĪŖ1+4”Į$\frac{1}{8}$=$\frac{3}{2}$£¬ĖłŅŌĀĮŌ×ÓÓėĢśŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ3£¬øĆĢśĀĮŗĻ½šµÄ»ÆѧŹ½ĪŖ£ŗAlFe3£¬
¹Ź“š°øĪŖ£ŗAlFe3£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°µē×ÓÅŲ¼Ź½”¢µēøŗŠŌ”¢¦Ņ¼üŹżŅŌ¼°¾§Ģå½į¹¹·ÖĪöµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāĶ¬Ņ»ÖÜĘŚÖŠµŚŅ»µēĄėÄܵıä»ÆĒ÷ŹĘ¼°Ņģ³£ĻÖĻó£¬ĪŖŅדķµć£®


 ±øÕ½ÖŠæ¼ŗ®¼ŁĻµĮŠ“š°ø
±øÕ½ÖŠæ¼ŗ®¼ŁĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 £Ø””””£©
£Ø””””£©| A£® | ¢Ł¢Ś | B£® | ¢Ś¢Ū | C£® | ¢Ū¢Ü | D£® | ¢Ł¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØX2£©=0.15 mol/L | B£® | c£ØY2£©=0.9 mol/L | C£® | c£ØZ2£©=0.3 mol/L | D£® | c£ØQ2£©=0.4 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 10mL 0.1mol/L Na2S2O3ČÜŅŗŗĶ10mL 0.1mol/LH2SO4ČÜŅŗ | |
| B£® | 5mL 0.1mol/L Na2S2O3ČÜŅŗŗĶ5mL 0.1mol/LH2SO4ČÜŅŗ | |
| C£® | 5mL 0.1mol/L Na2S2O3ČÜŅŗŗĶ5mL 0.05mol/LH2SO4ČÜŅŗ | |
| D£® | 10mL 0.5mol/L Na2S2O3ČÜŅŗŗĶ10mL 0.05mol/LH2SO4ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
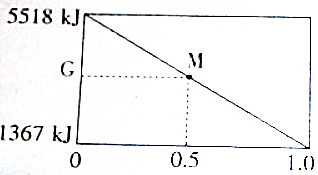 ÓŠX”¢YĮ½ÖÖŅŗĢ¬Č¼ĮĻ£¬Č”1molÓÉX”¢Y×é³ÉµÄ»ģŗĻĪļ£¬ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³É¶žŃõ»ÆĢ¼ŗĶŅŗĢ¬Ė®Ź±·Å³öČČĮæÓė»ģŗĻĪļXĪļÖŹµÄĮæ·ÖŹż[$\frac{n£ØX£©}{n£ØX£©+n£ØY£©}$]¹ŲĻµČēĶ¼ĖłŹ¾£®
ÓŠX”¢YĮ½ÖÖŅŗĢ¬Č¼ĮĻ£¬Č”1molÓÉX”¢Y×é³ÉµÄ»ģŗĻĪļ£¬ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³É¶žŃõ»ÆĢ¼ŗĶŅŗĢ¬Ė®Ź±·Å³öČČĮæÓė»ģŗĻĪļXĪļÖŹµÄĮæ·ÖŹż[$\frac{n£ØX£©}{n£ØX£©+n£ØY£©}$]¹ŲĻµČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ¾ŪŅŅĻ©ĖÜĮĻ“śĢę¾ŪČéĖįĖÜĮĻæɼõÉŁ°×É«ĪŪČ¾ | |
| B£® | ŗ¬ÖŲ½šŹōĄė×ӵĵē¶Ę·ĻŅŗ²»ÄÜĖęŅāÅÅ·Å | |
| C£® | “óĮæČ¼ÉÕ»ÆŹÆČ¼ĮĻŹĒŌģ³ÉĪķö²ĢģĘųµÄŅ»ÖÖÖŲŅŖŅņĖŲ | |
| D£® | Si3N4ŹĒŅ»ÖÖŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻ£¬æÉÓ¦ÓĆÓŚÖĘŌģ·¢¶Æ»ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 »„ĪŖĶ¬ĻµĪļ£®
»„ĪŖĶ¬ĻµĪļ£®
 £®
£® -CH2CH2CH2OH
-CH2CH2CH2OH £ØCH3£©2CHCOOCH2CH2CH2-
£ØCH3£©2CHCOOCH2CH2CH2- +H2O£®
+H2O£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢H+”¢S2O32-”¢PO43- | B£® | Pb2+”¢Hg2+”¢S2-”¢SO42- | ||
| C£® | Na+”¢Ba2+”¢Cl-”¢OH- | D£® | Ca2+”¢Fe3+”¢Br-”¢I- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C£ØCl-£©£¾C£ØNH4+£©£¾C£ØH+£©£¾C£ØOH-£© | B£® | C£ØCl-£©£¾C£ØNH4+£©£¾C£ØOH-£©£¾C£ØH+£© | ||
| C£® | C£ØCl-£©=C£ØNH4+£©£¾C£ØH+£©=C£ØOH-£© | D£® | C£ØNH4+£©=C£ØCl-£©£¾C£ØH+£©£¾C£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com