
| A. | 淀粉碘化钾试纸 | B. | 氯气 | C. | 氧气 | D. | 蒸馏水 |
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中只能含离子键 | B. | 共价化合物中可能含离子键 | ||
| C. | 共价键只存在于共价化合物中 | D. | 离子键只存在于离子化合物中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | .所有铵盐都溶于水 | |
| B. | 铵态氮肥与草木灰混合使用肥效更好 | |
| C. | .铵盐受热分解都会产生氨气 | |
| D. | .铵盐都能与碱反应,都不能与酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |
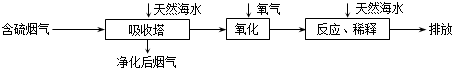
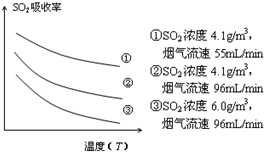
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
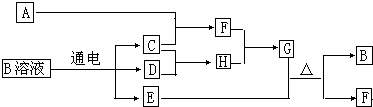
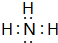 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚有腐蚀性,溅在皮肤上可用酒精冲洗 | |
| B. | 凡是分子中有-OH的化合物都是醇 | |
| C. | 苯酚是一种弱酸,滴加指示剂变色 | |
| D. | C6H5-OH与C6H5-CH2OH互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
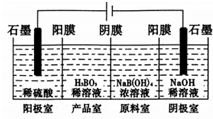
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
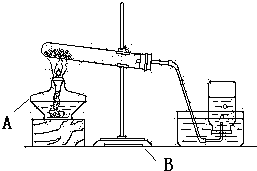
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com