
ŅŃÖŖĻĀĮŠČČ»Æѧ·½³ĢŹ½£ŗ
¢Ł Fe2O3(s) + 3CO(g) = 2Fe(s) + 3CO2(g) ”÷H= -25kJ”¤mol-1
¢Ś 3Fe2O3(s) + CO(g) = 2Fe3O4(s) + CO2(g) ”÷H= - 47kJ”¤mol-1
ŌņĻĀĮŠ¹ŲÓŚFe3O4(s)±»CO»¹Ō³ÉFe(s)ŗĶCO2µÄČČ»Æѧ·½³ĢŹ½µÄŹéŠ“ÖŠÕżČ·µÄŹĒ
A£®Fe3O4 + 4CO = 3Fe + 4CO2 ”÷H= -14kJ”¤mol-1
B£®Fe3O4(s) + 4CO(g) = 3Fe(s) + 4CO2(g) ”÷H= -22kJ”¤mol-1
C£®Fe3O4(s) + 4CO(g) = 3Fe(s) + 4CO2(g) ”÷H= +14kJ”¤mol-1
D£®Fe3O4(s) + 4CO(g) = 3Fe(s) + 4CO2(g) ”÷H= -14kJ”¤mol-1

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ø߶žĻĀѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹŹōÓŚ“æ¾»ĪļµÄŹĒ( )
A£®ø£¶ūĀķĮÖ B£®¾ŪŅŅĻ© C£®ĻĖĪ¬ĖŲ D£®Ó²Ö¬ĖįøŹÓĶõ„
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĖÄ“ØŹ”ø߶ž4ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲĄė×Ó¹²“ęµÄĖµ·Ø¼°Ļą¹Ų·ÖĪöÕżČ·µÄŹĒ£Ø £©
Ń”Ļī | Ąė×Ó×é | ·ÖĪö |
A | ŗ¬“óĮæAl3+µÄČÜŅŗÖŠ£ŗK+”¢Na+”¢NO3£”¢CO32£ | ²»ÄÜ“óĮæ¹²“ę£¬ŅņÓŠAl2(CO3)3³ĮµķÉś³É |
B | ŗ¬“óĮæFe3+µÄČÜŅŗÖŠ£ŗK+”¢Mg2+”¢I£”¢NO3£ | ²»ÄÜ“óĮæ¹²“ę£¬Ņņ2Fe3+ + 2I£=2Fe2++I2 |
C | ÓÉĖ®µēĄėµÄc(H+)=1”Į10-14mol/LµÄČÜŅŗÖŠ£ŗ Ca2+”¢NO3£”¢HCO3£”¢Cl£ | ²»ÄÜ“óĮæ¹²“ę£¬ŅņČÜŅŗ³ŹĖįŠŌ£¬ÓėHCO3£·“Ó¦²śÉśCO2ĘųĢå |
D | Ź¹·ÓĢŖ±äŗģµÄČÜŅŗÖŠ£ŗ Na+”¢K+”¢SO32£”¢S2£ | ²»ÄÜ“óĮæ¹²“ę£¬ŅņSO32£ŗĶS2£·“Ó¦²śÉśµ»ĘÉ«µÄS³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ĻĆĆÅŹŠø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŅŃÖŖ£ŗC(s)+2NO(g)  N2(g)+CO2(g)”£ T”ꏱ£®Ä³ŃŠ¾æŠ”×éĻņŅ»ŗćČŻÕęæÕČŻĘ÷ÖŠ³äČėNOŗĶ×ćĮæµÄĢ¼µ„ÖŹ£¬ŗćĪĀĢõ¼žĻĀ²āµĆ²»Ķ¬Ź±¼äø÷ĪļÖŹµÄÅضČČēĻĀ±ķ”£
N2(g)+CO2(g)”£ T”ꏱ£®Ä³ŃŠ¾æŠ”×éĻņŅ»ŗćČŻÕęæÕČŻĘ÷ÖŠ³äČėNOŗĶ×ćĮæµÄĢ¼µ„ÖŹ£¬ŗćĪĀĢõ¼žĻĀ²āµĆ²»Ķ¬Ź±¼äø÷ĪļÖŹµÄÅضČČēĻĀ±ķ”£
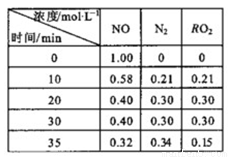
£Ø1£©0”«10minŅŌV(NO)±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ _”£
£Ø2£©øł¾Ż±ķÖŠŹż¾Ż£¬¼ĘĖćĘ½ŗāŹ±µÄNO×Ŗ»ÆĀŹĪŖ _”£
£Ø3£©øł¾Ż±ķÖŠŹż¾Ż£¬¼ĘĖćT”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ ”£
£Ø4£©30”«35 minøıäµÄŹµŃéĢõ¼žŹĒ _
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ĻĆĆÅŹŠø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
æŲÖĘŹŹŗĻµÄĢõ¼ž£¬½«·“Ó¦2Fe3+£«2I£ 2Fe2+£«I2Éč¼Ę³ÉČēÓŅĶ¼ĖłŹ¾µÄŌµē³Ų”£ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ
2Fe2+£«I2Éč¼Ę³ÉČēÓŅĶ¼ĖłŹ¾µÄŌµē³Ų”£ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ
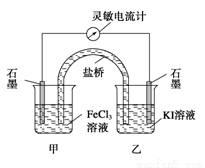
A£®·“Ó¦æŖŹ¼Ź±£¬ŅŅÖŠŹÆÄ«µē¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦
B£®·“Ó¦æŖŹ¼Ź±£¬¼×ÖŠŹÆÄ«µē¼«ÉĻµÄFe3£«±»»¹Ō
C£®µēĮ÷¼Ę¶ĮŹżĪŖĮ揱£¬·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬
D£®µēĮ÷¼Ę¶ĮŹżĪŖĮćŗó£¬ŌŚ¼×ÖŠČÜČėFeCl2¹ĢĢ壬ŅŅÖŠµÄŹÆÄ«µē¼«ĪŖøŗ¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ĻĆĆÅŹŠø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ1molĒāĘųĶźČ«Č¼ÉÕÉś³ÉĖ®ÕōĘųŹ±·Å³öČČĮæ242 kJ”£ĒŅŃõĘųÖŠ1 mol O£½O¼üĶźČ«¶ĻĮŃŹ±ĪüŹÕČČĮæ496 kJ£¬Ė®ÕōĘųÖŠ1 mol H£O¼üŠĪ³ÉŹ±·Å³öČČĮæ463 kJ£¬ŌņĒāĘųÖŠ1mol H£H¼ü¶ĻĮŃŹ±ĪüŹÕČČĮæĪŖ
A£®920 kJ B£®557 kJ C£®436 kJ D£®188 kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ĘĪĢļŹŠøßŅ»ĻĀѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ČēĶ¼ŹĒŹµŃéŹŅÖĘSO2²¢ŃéÖ¤SO2ijŠ©ŠŌÖŹµÄ×°ÖĆĶ¼£¬ŹŌ»Ų“š£ŗ
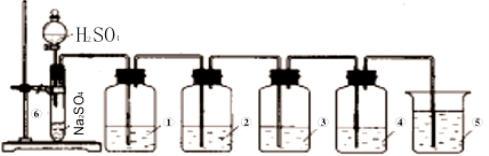
ŹÆČļŹŌŅŗ Ę·ŗģŹŌŅŗ H 2SŹŌŅŗ µāĖ®
(1)¢ŽŃĒĮņĖįÄĘŗĶÅØĮņĖį·“Ó¦·½³ĢŹ½ĪŖ
(2)¢ŁÖŠĻÖĻóĪŖ £¬Ö¤Ć÷SO2ŹĒ ĘųĢ唣
(3)¢ŚÖŠĘ·ŗģČÜŅŗ £¬Ö¤Ć÷SO2ÓŠ ”£
(4)¢ŪÖŠĻÖĻóŹĒ £¬Ö¤Ć÷SO2ÓŠ ŠŌ”£
(5)¢ÜÖŠĻÖĻóŹĒ £¬Ö¤Ć÷SO2ÓŠ ŠŌ”£
(6)¢ŻµÄ×÷ÓĆŹĒ £¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ĘĪĢļŹŠøßŅ»ĻĀѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŌĻĀ×Ŗ»Æ²»ÄÜĶعżŅ»²½·“Ó¦ŹµĻֵďĒ( )
A£®Al2O3”śAl(OH)3 B£®SiO2”śSiF4 C£®Fe”śFeCl2 D£®Na”śNaOH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹óÖŻŹ”ø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Čō1 molijĘųĢ¬ĢžCxHyĶźČ«Č¼ÉÕ£¬ŠčÓĆ3 mol O2£¬Ōņ £Ø £©
A£®x£½2£¬y£½2 B£®x£½2£¬y£½4 C£®x£½3£¬y£½6 D£®x£½3£¬y£½8
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com