
 关系相互转化的是( )
关系相互转化的是( )| 选项 | A | B | C | D |
| a | Fe | SiO2 | Al(OH)3 | HNO3 |
| b | FeCl3 | Na2SiO3 | NaAlO2 | NO |
| c | FeCl2 | H2SiO3 | Al2O3 | NO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据物质的性质判断反应能否发生,C中Al2O3不能与水反应生成Al(OH)3.
解答 解:A、Fe$\stackrel{Cl_{2}}{→}$FeCl3$\stackrel{Fe}{→}$FeCl2$\stackrel{Zn}{→}$Fe,可以一步实现,故A不符合;
B、SiO2$\stackrel{NaOH}{→}$Na2SiO3 $\stackrel{HCl}{→}$H2SiO3$\stackrel{△}{→}$SiO2,故B不符合;
C、Al(OH)3$\stackrel{NaOH}{→}$NaAlO2,不能一步实现生成Al2O3,Al2O3不能一步实现生成Al(OH)3,故C符合;
D、HNO3$\stackrel{Cu}{→}$NO$\stackrel{O_{2}}{→}$NO2$\stackrel{H_{2}O}{→}$HNO3,故D不符合;
故选C.
点评 本题考查元素化合物知识,题目难度不大,本题注意把握常见元素化合物的性质.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | 只有②④ | C. | ①②④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为 890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol | |
| B. | 500℃、30 MPa 下,将 0.5 mol N2 和 1.5 mol H2 置于密闭的容器中充分反应生成 NH3(g),放热 19.3 kJ,其热化学方程式为 N2(g)+3H2(g)?2NH2(g)△H=-38.6 kJ•mol | |
| C. | 一定条件下,反应 N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol降低温度将向正反应方向移动 | |
| D. | 已知 2C(s)+2O2(g)═2CO2(g)△H12C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人体内没有能使纤维素水解成葡萄糖的酶,因此纤维素不能作为人类的营养食物 | |
| B. | 严重影响我国北方的霾尘,其颗粒物是种胶体 | |
| C. | 大力实施矿物燃料“脱硫、脱硝技术”,可减少硫的氧化物和氮的氧化物对环境的污染 | |
| D. | 自来水厂常加入FeSO4和Cl2处理水,达到同时杀菌、消毒和聚沉水体中悬浮物的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,取pH=2的 HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )
常温下,取pH=2的 HA溶液与HB溶液各1mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示.下列叙述正确的是( )| A. | 稀释前,c(HB)>c(HA)=0.01 mol•L-1 | |
| B. | HB的电离方程式为HB=H++B- | |
| C. | NaA的水溶液中,离子浓度大小为:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| D. | NaA、NaB的混合溶液中:2c(Na+)=c(A-)+c(B-)+c(HB) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液溴易挥发,应用水液封并放在冷暗处保存 | |
| B. | 金属钠遇到氧气立即反应,应保存在煤油中或者液体石蜡里 | |
| C. | 硝酸见光易分解,应用棕色广口试剂瓶保存 | |
| D. | 碳酸钠虽然属于盐,但是其水溶液呈碱性,应用带橡胶塞的试剂瓶保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
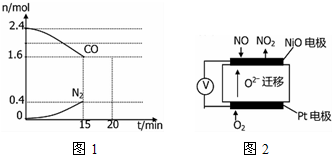
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫在空气中燃烧,产生蓝紫色火焰 | |
| B. | 将二氧化碳通入水中,无明显现象 | |
| C. | 红亮的铜丝在酒精灯火焰上灼烧,铜丝表面变黑 | |
| D. | 一氧化碳通过灼热的氧化铁,红色固体变黑 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com