
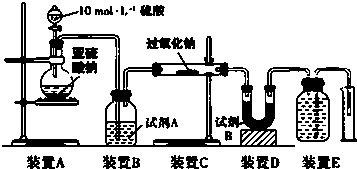
���� ����ʵ��װ�ÿ�֪����Ũ�������������Ʒ�Ӧ���ɶ������������ͨ��������ƣ���ͨ����ʯ������δ��Ӧ�Ķ�������������ˮ������������Ӧ���ɵ���������Ϲ���ijɷݷ�����Ӧ��ԭ������1�����ݼ���һ�ͼ�����ƶϼ�����ΪNa2SO3��Na2SO4�Ļ����ó����ۼ��ɣ�
��2���������ƺ�ˮ��Ӧ��װ��A���Լ�������ˮ�����������Լ�ΪŨ���ᣬ���������ȥˮ�������Լ�B��ȥ������SO2��
��3����Na2SO3δ�����������ķ�Ӧֻ��2Na2O2+2SO2=2Na2SO3+O2���ݲ��������㼴�ɣ�
��4����SO2��ȫ���������ɹ����������ƣ�
��� �⣺����ʵ��װ�ÿ�֪����Ũ�������������Ʒ�Ӧ���ɶ������������ͨ��������ƣ���ͨ����ʯ������δ��Ӧ�Ķ�������������ˮ������������Ӧ���ɵ���������Ϲ���ijɷݷ�����Ӧ��ԭ������1������ΪNa2SO3��Na2SO4�Ļ���֤��SO2���ֱ�������
�ʴ�Ϊ��Na2SO3��Na2SO4�Ļ���SO2���ֱ�������
��2���������ƺ�ˮ��Ӧ��װ��A���Լ�������ˮ�����������Լ�ΪŨ���ᣬ���������ȥˮ������װ��BΪ�ⶨ�����������������Ҫ��ʣ��Ķ��������ȥ��ʵ��Bװ������������δ��Ӧ��SO2��
�ʴ�Ϊ��Ũ�������δ��Ӧ��SO2��
��3��ʵ����װ��C�й�����������������m1 g��װ��D����������m2 g��װ��E���ռ���������ΪV L���ѻ���ɱ�״���£�����SO2δ��������
������Ӧ��2Na2O2+2SO2=2Na2SO3+O2
���ݻ�ѧ����ʽ�ͷ�Ӧ���ؼ���E���ռ���������
2Na2O2+2SO2=2Na2SO3+O2 ��Ӧ����
1mol 96g
$\frac{VL}{22.4L/mol}$ m1g
��ã�V=$\frac{7{m}_{1}}{30}$L
��SO2ȫ�������������ķ�ӦΪ��Na2O2+SO2=Na2SO4����Ӧ���������������ɣ�V=0����0��V��$\frac{7{m}_{1}}{30}$����SO2���ֱ�������
�ʴ�Ϊ��V=$\frac{7{m}_{1}}{30}$L��V=0��
��4����SO2��ȫ����������Ӧ�Ļ�ѧ����ʽΪ��SO2+Na2O2�TNa2SO4��
�ʴ�Ϊ��SO2+Na2O2�TNa2SO4��
���� ���⿼���˶�����������Ӧ�ú�ʵ����֤��ʵ����ƵIJ����ʵ�鷽����ȷ��Ӧ�������Ҫ������жϣ��ؼ��Ƕ��������Ϣ������������������жϣ���Ŀ���ѣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E������A��B��C��ͬһ���ڵķǽ���Ԫ�أ�������DCΪ���ӻ����D�Ķ�����������C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ��AC2Ϊ���������壬ͨ�����ʯ��ˮ�У�ʯ��ˮ����ǣ�B��C���⻯��ķе������ͬ����������Ԫ���⻯��ķе�ߣ�EԪ���ڵؿ��к���λ�ӵ���λ��ECl3����B��C���⻯���γ�����λ��������������������ʵ���֮��Ϊ2��1������������λ����磮���������������ش��������⣺������ʱ��A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ��
��֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E������A��B��C��ͬһ���ڵķǽ���Ԫ�أ�������DCΪ���ӻ����D�Ķ�����������C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ��AC2Ϊ���������壬ͨ�����ʯ��ˮ�У�ʯ��ˮ����ǣ�B��C���⻯��ķе������ͬ����������Ԫ���⻯��ķе�ߣ�EԪ���ڵؿ��к���λ�ӵ���λ��ECl3����B��C���⻯���γ�����λ��������������������ʵ���֮��Ϊ2��1������������λ����磮���������������ش��������⣺������ʱ��A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�23g NO2��N2O4�Ļ�������к���NA����ԭ�� | |
| B�� | �����£�pH=1��H2SO4��Һ�к��е�H+����ĿΪ0.1NA | |
| C�� | ��״���£�2.24L SO3�к�����ԭ�ӵ���ĿΪNA | |
| D�� | ��״���£�22.4L Cl2��ȫ����ˮʱ��ת�Ƶ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Na2SiO3��Һ�еμӷ�̪����Һ��죬֤��Na2SiO3������ˮ�ⷴӦ | |
| B�� | �������ھƾ��ƻ����ϼ��ȣ������ۻ��������䣬֤���������۵������ | |
| C�� | ��HClO��Һ��ͨ��SO2������H2SO4��֤��H2SO4�����Ա�HClOǿ | |
| D�� | ��������ˮ�ε���ɫʯ����ֽ�ϣ���ֽ�ȱ�����ɫ��֤����ˮ��Ư���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������������Al+2H+�TAl3++H2�� | |
| B�� | ̼��þ���������У�2H++CO32-�TCO2��+H2O | |
| C�� | �ڳ����ʯ��ˮ��ͨ��������CO2��Ca2++2OH-+CO2�TCaCO3��+H2O | |
| D�� | �����Ȼ�����Һ�����ˮ�У�Fe3++3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3��+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������pH=7����Һ�У�Fe3+��Mg2+��SO42-��Cl-�ܴ������� | |
| B�� | ������ˮ�����c��H+����c��OH-��=10-10����Һ�У�Na+��NH4+��CH3COO-��F-���ܴ������� | |
| C�� | �ں���HCO3-��HSO3-��CH3COO-��S2-���������ӵ���Һ�м����㹻��Na2O2�����S2-Ũ�ȱ仯��С | |
| D�� | SO2��O2��HCl��CO2�������壬���Դ���������ͬһ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
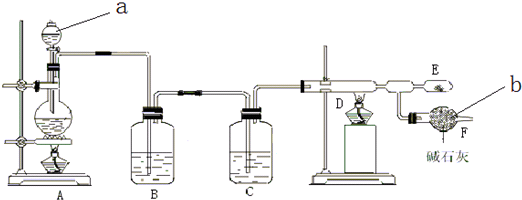
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
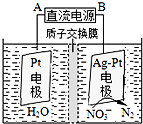 Ϊ����������������������ҵ��ͨ�������з�������CO2�������������Ⱦ��
Ϊ����������������������ҵ��ͨ�������з�������CO2�������������Ⱦ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com