
| A、Cl2>I2>Fe3+ |
| B、Cl2>Fe3+>I2 |
| C、Fe3+>Cl2>I2 |
| D、I2>Cl2>Fe3+ |


科目:高中化学 来源: 题型:
| A、含有AlO2-的溶液中:Na+、Al3+、NO3-、Cl- |
| B、使淀粉碘化钾变蓝的溶液中:K+、HCO3-、S2-、SO42- |
| C、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Fe3+ |
| D、透明溶液中:Na+、MnO4-、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
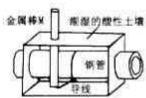 全世界短年钢铁因锈蚀造成大量的损失.某城市拟用如图所示方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀.关于此方法,下列说法不正确的是( )
全世界短年钢铁因锈蚀造成大量的损失.某城市拟用如图所示方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀.关于此方法,下列说法不正确的是( )| A、土壤中的钢铁易被腐蚀是因为在潮湿的土壤中形成了原电池 |
| B、金属棒X的材料应该是比镁活泼的金属 |
| C、金属棒X上发生反应:M-ne---Mn+ |
| D、这种方法称为牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、它们都是吸热反应 |
| B、a,b和c均为负值 |
| C、a=b |
| D、2b=c>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电子总数 | B、质子总数 |
| C、分子总数 | D、氮原子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、A、B、C三者中,A为金属性元素,B、C为非金属性元素 |
| B、A、B、C三者核电荷数之和为40 |
| C、A与B、A与C均可形成离子化合物 |
| D、B与C只能形成一种共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组测定某Fe2(SO4)3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:
某化学兴趣小组测定某Fe2(SO4)3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com