
【题目】已知2A2(g)+B2(g)![]() 2C(g) ΔH=-a kJ·mol-1(a > 0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
2C(g) ΔH=-a kJ·mol-1(a > 0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
(1)a___(填“>”“=”或“<”)b。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将__(填“增大”“减小”或“不变”)。
(3)若在原来的容器中,只加入2 mol C,500 ℃时充分反应达到平衡后,吸收热量c kJ,C的浓度___(填“>”“=”或“<”)w mol·L-1。
(4)能说明该反应已经达到平衡状态的是___。(填序号,下同)
a.v(C)=2v(B2) b.容器内压强保持不变
c.v逆(A2)=2v正(B2) d.容器内气体的密度保持不变
(5)使该反应的反应速率增大,且平衡向正反应方向移动的操作是___;能使B的转化率增大的操作是________;使平衡向逆反应方向移动的操作是________。
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d..选择高效的催化剂
【答案】> 减小 = bc c a b
【解析】
(1)热化学方程式表达的意义为:当2mol A2和1mol B2完全反应时,放出热量为akJ,而加入2mol A2和1mol B2达到平衡时,没有完全进行,即释放的热量小于完全反应释放的热量,即a>b;
(2)正反应方向放热,升高温度,化学平衡向逆反应方向移动,生成物浓度减小,反应物浓度增大,K减小;
(3)在同一容器同一条件下 2molA2和1molB2建立的平衡和2mol C建立的平衡是等效平衡。所以平衡后C的浓度仍为w mol/L,答案为“=”;
(4)a.v(C)=2v (B2),从反应开始平衡一直有这样的等量关系,所以不能作平衡状态的标志,选项a错误;
b.容器内压强保持不变,说明总物质的量不变,正逆反应速率相等,选项b正确;
c.v逆(A2)=2v逆(B2)=2v正(B2),说明达平衡状态,选项c正确;
d.容器内的密度保持不变,从反应开始平衡一直有这样的等量关系,所以不能作平衡状态的标志,选项d错误;答案选bc;
(5)为使该反应的反应速率增大,且平衡向正反应方向移动,则a.及时分离出C气体,生成物浓度减小,反应速率减小,平衡正向进行,故a错误b.反应是放热反应,适当升高温度,反应速率增大,平衡逆向进行,故b错误;c.增大B2的浓度,增大反应速率,平衡正向进行,故c正确;d.选择高效的催化剂改变反应速率但不改变化学平衡,故d错误;故答案选c;
能使B2的转化率增大则平衡正向移动,a.及时分离出C气体,平衡正向移动,B2的转化率增大,故正确;b.适当升高温度,平衡向吸热反应的逆方向移动,B2的转化率减小,故错误;c.增大B2的浓度,平衡正向移动,但因B2增加的的量比平衡移动转化的B2量大得多,故B2的转化率反而减小,故错误;d..选择高效的催化剂,平衡不移动,B2的转化率不变,故错误;答案选a;
使平衡向逆反应方向移动,a.及时分离出C气体,平衡正向移动,故错误;b.适当升高温度,平衡向吸热反应的逆反应方向移动,故正确;c.增大B2的浓度,平衡正向移动,故错误;d..选择高效的催化剂,平衡不移动,故错误。答案选b。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】随着汽车数量的逐年增多,汽车尾气污染已成为突出的环境问题之一。反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是( )
A.提高尾气净化效率的最佳途径是研制高效催化剂
B.提高尾气净化效率的常用方法是升高温度
C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
D.570 K时及时抽走CO2、N2,平衡常数将会增大,尾气净化效率更佳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为_________________个。
(2)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为____________。(水的密度为1g/mL)
(3)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.石油裂化、裂解和分馏均为化学变化
B.煤焦油中可以分离出苯、甲苯、二甲苯等有机化合物
C.利用CO2制造全降解塑料能有效减少环境污染
D.生物质能来源于植物及其加工产品所贮存的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,均属于共价化合物并且化学键类型完全相同的是( )
A. O2和CCl4B. NaH和HIC. Cl2和NH4NO3D. CCl4和H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
(1)水质优劣直接影响人体健康.天然水在净化处理过程中加入的混凝剂可以是 (填两种物质的名称),其净水作用的原理是
(2)水的净化与软化的区别是
(3)硬度为1°的水是指每升水含10mg CaO或与之相当的物质(如7.1mg MgO).若某天然水中c(Ca2+)=1.2×10﹣3mol/L,c(Mg2+)=6×10﹣4mol/L,则此水的硬度为 .
(4)若(3)中的天然水还含有c(HCO3﹣)=8×10﹣4mol/L,现要软化10m3这种天然水,则需先加入Ca(OH)2 克,后加入Na2CO3 克.
(5)如图是电渗析法淡化海水的原理图,其中,电极A接直流电源的正极,电极B接直流电源的负极.

①隔膜A是 (填“阴”或“阳”)离子交换膜;
②某种海水样品,经分析含有大量的Na+、Cl﹣,以及少量的K+、SO42﹣.若用上述装置对该海水进行淡化,当淡化工作完成后,A、B、C三室中所得溶液(或液体)的pH分别为pHa、pHb、pHc,则其大小顺序为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL0.3mol/LNa2SO4溶液和100mL0.2mol/LAl2(SO4)3溶液混合后,溶液中SO42-的物质的量浓度约为:( )
A. 0.2mol/LB. 0.25mol/LC. 0.45mol/LD. 0.50mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应H2(g)+I2(g)![]() 2HI(g) ΔH<0,在一带有活塞的密闭容器中达到平衡,下列说法不正确的是 ( )
2HI(g) ΔH<0,在一带有活塞的密闭容器中达到平衡,下列说法不正确的是 ( )
A. 恒温,压缩体积,平衡不移动,颜色加深
B. 恒压,迅速充入HI,开始时正反应速率减小
C. 恒容,升温逆反应速率增大,正反应速率减小
D. 恒容,充入H2,I2转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组欲探究SO2与Cu(OH)2 的反应。
实验 | 实验步骤 | 现象 |
| 步骤1:打开分液漏斗,向烧瓶中加入30mL 0.5 mol/LNaOH溶液 | I. 有蓝色絮状沉淀,静置后分层。 |
步骤2:从左侧导管通入SO2气体 | II. 静置后分层,上层溶液为淡绿色,底部有白色沉淀 |
(1)现象I中产生蓝色沉淀的离子方程式是___________。
(2)甲为了确认现象II中白色沉淀的成分,进行如下探究。查阅资料:
CuSO3 | CuCl | Cu2O | |
溶解性 | 不溶于水,浅黄色沉淀 | 不溶于水,白色沉淀 | 不溶于水,砖红色沉淀 |
性质 | 与酸反应 | 能溶于较浓的HCl溶液 | 酸性体系中不稳定,进一步反应生成Cu和Cu2+ |
并进行如下实验:
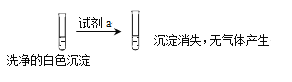
①试剂a是___________。
②现象II中生成白色沉淀的离子方程式是___________。
(3)甲认为Cu(OH)2沉淀全部转化为CuCl,乙依据实验现象对甲的观点进行反驳,依据的实验现象是_________。
(4)丙认为实验存在干扰,欲探究纯净的Cu(OH)2 悬浊液与SO2的反应。
①丙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,_________(填操作和现象),证明已洗涤干净。再进行如下实验:
实验 | 实验步骤 | 现象 |
| 从左侧导管通入SO2气体 | III. 静置后分层,上层溶液为淡绿色,底部有砖红色沉淀。 |
②丙预测产物是Cu2O,取砖红色沉淀,洗涤后,_________(填操作和现象),证明产物是Cu2O。
(5)纯净的Cu(OH)2 悬浊液与SO2发生反应的化学方程式是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com