
| 物质 | 氢气 | 原煤 (主要成份是C) | 汽油 (主要成份C8H18) |
| 热量(kJ) | 285.8 | 250.9 | 4910 |
分析 (1)1molH2完全燃烧放出的热量为:285.8kJ,所以热化学方程式是2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol;
(2)电解饱和食盐水,依据电极反应判断生成产物,书写离子方程式.
解答 解:(1)1molH2完全燃烧放出的热量为:285.8kJ,所以热化学方程式是2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol,故答案为:2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol;
(2)电解饱和食盐水,溶液中的氯离子在阳极失电子生成氯气,氢离子在阴极得到电子生成氢气,阴极附近氢氧根离子浓度增大生成氢氧化钠,反应的离子方程式:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑.
点评 本题考查了热化学方程式和电解方程式的书写,掌握基础是关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
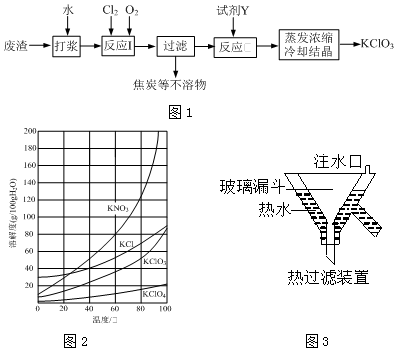
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉、Cl2、氨水、NaHCO3 | B. | 福尔马林、苯、Cu2(OH)2CO3、明矾 | ||
| C. | 盐酸、SO2、纯碱、NH4Cl | D. | 食醋、C2H5OH、苛性钾、NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
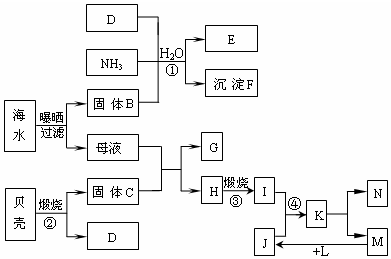
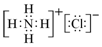 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g NH3含有电子数为10NA | |
| B. | 标况下,4.48LH2O中所含的分子数是0.2NA | |
| C. | 0.1mol/L的K2SO4溶液中,K+的数目为0.2NA | |
| D. | 30 g乙烷(C2H6)所含的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.96% | B. | 5.66% | C. | 75% | D. | 12.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol | B. | 2H2(g)+O2(g)═2H2O(1)△H=+571.6 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.8kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com