
| A. | Zn为正极,Cu为负极,CuCl2溶液作为电解质溶液 | |
| B. | Zn为负极,Cu为正极,稀H2SO4溶液作为电解质溶液 | |
| C. | Zn为负极,Cu为正极,CuSO4溶液作为电解质溶液 | |
| D. | Zn为负极,Fe为正极,Zn发生还原反应 |
分析 根据电池反应式知,失电子的金属作负极,则锌作负极,不如负极活泼的金属或导电的非金属作正极,铜离子得电子发生还原反应,所以电解质溶液中含有铜离子,则电解质溶液为可溶性的铜盐.
解答 解:根据电池反应式Zn+Cu2+=Zn2++Cu知,锌失电子发生氧化反应而作负极,不如负极活泼的金属或导电的非金属作正极,正极上Cu2+得电子发生还原反应,则电解质溶液中含有Cu2+,所以电解质溶液为可溶性的铜盐,
A.Zn为负极,铜为正极,故A错误;
B.应该是硫酸铜或氯化铁溶液为电解质溶液,故B错误;
C.Zn为负极,Cu为正极,CuSO4溶液作为电解质溶液,满足条件,故C正确;
D.负极锌失去电子发生氧化反应,故D错误;
故选C.
点评 本题考查了原电池工作原理,为高频考点,答题时注意判断正负极、电解质溶液时,要根据电池反应式判断:发生氧化反应的电极为负极,发生还原反应的电极为正极,含有发生还原反应的离子溶液为电解质溶液,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | pH=3的溶液 | B. | c(H+)=1×10-5mol/L的溶液 | ||
| C. | c(OH-)=1×10-12 mol/L的溶液 | D. | 0.005 mol/L的H2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
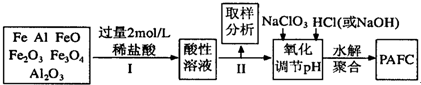
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
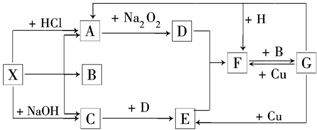
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N5+具有34个电子 | B. | N5+中氮-氮之间是以共价键结合 | ||
| C. | 化合物N5AsF6中As的化合价为+1 | D. | 化合物N5AsF6中F的化合价为-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知中和热为57.3kJ/mol,则HCl+NaOH═NaCl+H2O△H=-57.3kJ/mol | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)△H=+2×283.0kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3++3H2O?Fe(OH)3↓+3H+ | B. | NH4++2H2O?NH3•H2O+H3O+ | ||
| C. | CH3COOH+H2O?CH3COO-+H3O+ | D. | Br-+H2O?HBr+OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com