
【题目】我国濒临海域的省份,能够充分利用海水制得多种化工产品。如图是以海水、贝壳(主要成分CaCO3)等为原料制取几种化工产品的工艺流程图,其中E是一种化肥,N是一种常见的金属单质。
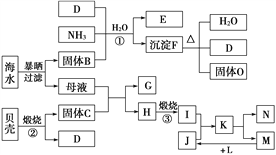
结合上述工艺流程图回答下列问题:
(1)物质G和L的化学式分别为________和________________。
(2)上述工艺流程图中可以循环使用的物质的化学式为______。
(3)反应①的化学方程式为______________________________;在反应①中必须先通入NH3,而后通入D,其原因是____________________。
(4)工业上利用F可制得另一种化工产品,该反应的化学方程式为________________。
(5)由K溶液经如何处理才能制得N?_____________________。
【答案】 CaCl2 H2 CO2 NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl NH3在溶液中的溶解度大,利于吸收CO2,使其转化为NaHCO3 2NaHCO3![]() Na2CO3+CO2↑+H2O MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,电解熔融MgCl2可制取金属镁
Na2CO3+CO2↑+H2O MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,电解熔融MgCl2可制取金属镁
【解析】题中的工艺流程图由海水晒盐、海水提镁和工业制纯碱三部分组成。分析工艺流程图中的转化关系可得B、C、D、E、F、G、H、I、J、K、L、M、N、O分别是NaCl、CaO、CO2、NH4Cl、NaHCO3、CaCl2、Mg(OH)2、MgO、HCl、MgCl2、H2、Cl2、Mg、Na2CO3。则
(1)根据以上分析可知物质G和L的化学式分别为CaCl2、H2。(2)在用贝壳制生石灰的同时生成CO2,在将NaHCO3加热分解制纯碱时也生成CO2,CO2可循环利用。(3)反应①是用NaCl、NH3、CO2和H2O反应制取NaHCO3和NH4Cl的反应,化学方程式为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl。NH3在水溶液中的溶解度大,利于吸收较多量的CO2使其转化为NaHCO3。(4)工业上用NaHCO3受热分解可制得纯碱,化学方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O。(5)氯化镁易水解生成氢氧化镁和氯化氢,加热促进水解,因此MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,再电解熔融MgCl2可制得金属镁。
Na2CO3+CO2↑+H2O。(5)氯化镁易水解生成氢氧化镁和氯化氢,加热促进水解,因此MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,再电解熔融MgCl2可制得金属镁。


科目:高中化学 来源: 题型:
【题目】下图是以黄铜矿(主要成分为CuFeS2)为原料制取胆矾晶体的流程:
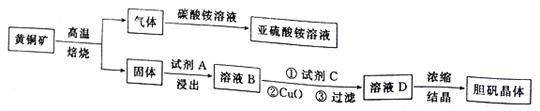
已知:
ⅰ.高温焙烧时的主要反应有:2CuFeS2+O2![]() Cu2S+2FeS+SO2
Cu2S+2FeS+SO2
2Cu2S+ 5O2![]() 2CuO+2CuSO4,2FeS+3O2
2CuO+2CuSO4,2FeS+3O2![]() 2FeO+2SO2 ;
2FeO+2SO2 ;
ⅱ.常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Cu(OH)2]=3.0×10-20。
(1)CuFeS2中硫元素的化合价为______________________,写出上述流程中生成亚硫酸铵的化学方程式:______________________________________________________________________。
(2)最适合的试剂A是__________(写化学式)溶液;当试剂A的浓度为6.0mol·L-1时 ,“浸出”实验中,铜的浸出率结果如下图所示。由图可知,当铜的浸出率为90% 时,所采用的实验条件(温度、时间)为__________。
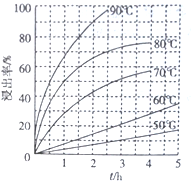
(3)最适合的试剂C是__________(填标号)。
a.Cl2b. H2O2 溶液 c.酸性高锰酸钾溶液 d.浓硫酸
(4)加入适量CuO粉末的作用是调节溶液的pH,促进Fe3+水解,达到除杂的目的。写出实现该目的的总反应的离子方程式:_________________________________________________________。
(5)有同学怀疑CuO不一定能达到上述目的,而小张同学却认为可以通过计算来确定。设溶液中Cu2+的浓度为3.0 mol·L-1,则Cu2+开始沉淀时溶液的pH 为__________,Fe3+沉淀完全时溶液的pH 为__________。通过计算判断加入CuO__________(填“能”或“不能”)达到目的(提示:1g 5=0.7;通常认为残留在溶液中的某离子浓度小于1.0×10-5 mol·L-1 时,就认为该离子已沉淀完全)。
(6)假设流程图中消耗的CuO为ag,最终制得bg胆矾晶体,消耗黄铜矿的质量为cg,不考虑生产过程中的损失,则黄铜矿中CuFeS2的质量分数为__________(写出原始的计算结果即可,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分元素在元素周期表中位置,根据下列要求回答问题:
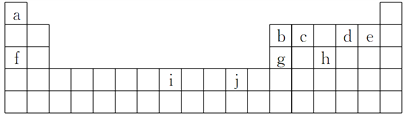
(1)下列关于Ca、97Bk(锫)、![]() Uus和
Uus和![]() Uus的说法中不正确的是____(填字母,下同)。
Uus的说法中不正确的是____(填字母,下同)。
A.117号元素的相对原子质量为293.5
B.![]() Uus和
Uus和![]() Uus互为同位素
Uus互为同位素
C. Ca、97Bk表示两种原子、两种元素
D.上述元素都位于长周期中
(2)根据元素周期表结构推知,117号元素在周期表中的位置是________。
A.第七周期第ⅣA族
B.第七周期第ⅦA族
C.第六周期第ⅣA族
D.第六周期第ⅦA族
(3)117号元素Uus属于________(填“金属元素”或“非金属元素”),它的气态氢化物稳定性比砹的气态氢化物稳定性________(填“强”或“弱”);它的最高价氧化物的化学式为________________。
(4)下列关于上述元素及其化合物的判断正确的是________(填字母)。
A.53I、55Cs和55Cs放射性元素变成其他元素,发生了化学变化
B.he3分子和ha3分子结构相同
C.j元素与d元素组成化合物的颜色相同
D.加碘食盐中“碘”不是碘53I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定烟雾中的SO2含量,可做下列实验:取100 L该烟雾(标准状况),通过盛放100 mL过氧化氢(H2O2)水溶液的吸收瓶,使它们充分反应,生成硫酸。在吸收后的水溶液中加入BaCl2溶液,生成白色沉淀,经测定其质量为11.65 g,则该烟雾中SO2的体积分数是( )
A. 1.12% B. 2.24%
C. 3.36% D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤是一种常用的燃料。由于煤燃烧产生的废气中含有SO2、NO2和NO等多种有害气体和烟尘,会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放。
(1)将煤直接进行燃烧可能会形成硝酸型酸雨。
①写出有关物质转化为硝酸的化学方程式_________________。
②以下是对硝酸型酸雨的评价,其中正确的是________(用序号填空)。
a.杀死水中的浮游生物,减少鱼类食物来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.破坏臭氧层,导致臭氧空洞
d.硝酸与土壤中的矿物质发生作用转化为硝酸盐,给植物提供氮肥
(2)如图是对煤燃烧产生的废气进行常温脱硫处理的基本流程示意图,试写出在废气脱硫并形成副产物的过程中所发生的主要化学反应的化学方程式_______________。
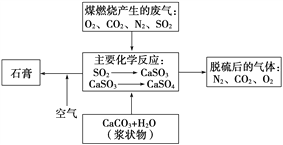
(3)脱硫以后,在废气中含量明显增加的不良气体是(写物质名称)________,它对环境的负面影响是___________________________________________。
(4)检验脱硫后废气中是否含有SO2的简单方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上测量SO2、N2、O2混合气体中SO2含量的装置如右图。反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2 +2H2O==H2SO4+2HI
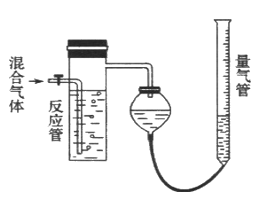
(1)混合气体进入反应管后,量气管内增加的水的体积等于__________的体积(填分子式)。
(2)反应管内的溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_____(填“偏高”、“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用_______________代替(填写物质名称)。
(4)若碘溶液体积为V![]() mL,浓度为cmol·L
mL,浓度为cmol·L![]() 。N2与O2的体积为V
。N2与O2的体积为V![]() mL(已折算为标准状况下的体积)。用c、V
mL(已折算为标准状况下的体积)。用c、V![]() 、V
、V![]() 表示SO2的体积百分含量为:_________________。
表示SO2的体积百分含量为:_________________。
(5)将上述装置改为简易实验装置,除导管外,还需选的仪器为________(选下列仪器编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验事实不能用平衡移动原理解释的是( )
A.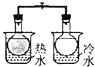 将NO2球浸泡在冷水和热水中
将NO2球浸泡在冷水和热水中
B.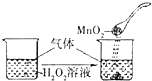 向H2O2溶液中滴加MnO2粉末
向H2O2溶液中滴加MnO2粉末
C.
T(℃) | 25 | 50 | 100 |
水的离子积常数KW(×10﹣14) | 1.01 | 5.47 | 55.0 |
D.
c(氨水)/mol.L﹣1 | 0.1 | 0.01 |
pH | 11.1 | 10.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质反应后一定有+3价铁生成的是
① Fe(过量)在Cl2燃烧;② Fe与过量稀H2SO4反应;③ Fe(NO3)2溶液中加少量盐酸;④ FeO和Fe2O3的混合物溶于盐酸中
A. ① ② ④ B. ① ③ ④ C. ① ② ③ D. ② ③ ④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com